какая кислота называется концентрированной
Какая кислота называется концентрированной
H 2 SO 3 сернистая
H 2 S сероводородная
H 2 SiO 3 кремниевая
H 3 PO 4 фосфорная
** Термин “одноосновная кислота” возник потому, что для нейтрализации одной молекулы такой кислоты требуется “одно основание”, т.е. одна молекула какого-либо простейшего основания типа NaOH или KOH:
HNO 3 + NaOH = NaNO 3 + H 2 O
HCl + KOH = KCl + H 2 O
Двухосновная кислота требует для своей нейтрализации уже “два основания”, а трехосновная – “три основания”:
H 2 SO 4 + 2 NaOH = Na 2 SO 4 + 2 H 2 O
H 3 PO 4 + 3 NaOH = Na 3 PO 4 + 3 H 2 O
Рассмотрим важнейшие химические свойства кислот.
Индикаторы представляют собой вещества сложного строения. В растворах оснований и в нейтральных растворах они имеют иную окраску, чем в растворах кислот. Об индикаторах мы более подробно расскажем в следующем параграфе на примере их реакций с основаниями.
Для реакций нейтрализации достаточно, чтобы хотя бы одно из реагирующих веществ было растворимо в воде. Поскольку практически все кислоты растворимы в воде, они вступают в реакции нейтрализации не только с растворимыми, но и с нерастворимыми основаниями. Исключением является кремниевая кислота, которая плохо растворима в воде и поэтому может реагировать только с растворимыми основаниями – такими как NaOH и KOH:
H 2 SiO 3 + 2 NaOH = Na 2 SiO 3 + 2H 2 O
Как и в случае реакций с основаниями, с основными оксидами кислоты образуют соль и воду. Соль содержит кислотный остаток той кислоты, которая использовалась в реакции нейтрализации.
Во-первых, металл должен быть достаточно активным (реакционноспособным) по отношению к кислотам. Например, золото, серебро, медь, ртуть и некоторые другие металлы с выделением водорода с кислотами не реагируют. Такие металлы как натрий, кальций, цинк – напротив – реагируют очень активно с выделением газообразного водорода и большого количества тепла.
По реакционной способности в отношении кислот все металлы располагаются в ряд активности металлов (табл. 8-3). Слева находятся наиболее активные металлы, справа – неактивные. Чем левее находится металл в ряду активности, тем интенсивнее он взаимодействует с кислотами.
Табл. 8-3. Ряд активности металлов.
Металлы, которые вытесняют водород из кислот
Металлы, которые не вытесняют водород из кислот
K Ba Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb (H)
¬ самые активные металлы
самые неактивные металлы ®
Например, кислоты растений (яблочная, лимонная, щавелевая и т.д.) являются слабыми кислотами и очень медленно реагируют с такими металлами как цинк, хром, железо, никель, олово, свинец (хотя с основаниями и оксидами металлов они способны реагировать).
С другой стороны, такие сильные кислоты как серная или соляная (хлороводородная) способны реагировать со всеми металлами из левой части табл. 8-3.
В связи с этим существует еще одна классификация кислот – по силе. В таблице 8-4 в каждой из колонок сила кислот уменьшается сверху вниз.
Таблица 8-4. Классификация кислот на сильные и слабые кислоты.
H 3 PO 4 фосфорная
H 2 SO 3 сернистая
H 2 S сероводородная
H 2 SiO 3 кремниевая
Cu + 4 HNO 3 (конц.) =Cu(NO 3 ) 2 + 2 NO 2 + 2 H 2 O
3 Cu + 8HNO 3 (разб.) = 3 Cu(NO 3 ) 2 + 2 NO + 4 H 2 O
8 K + 5 H 2 SO 4 ( конц.) = 4 K 2 SO 4 + H 2 S + 4 H 2 O
3 Zn + 4 H 2 SO 4 (конц.) = 3 ZnSO 4 + S + 4 H 2 O
Есть металлы, которые реагируют с разбавленными кислотами, но не реагирует с концентрированными (т.е. безводными ) кислотами – серной кислотой и азотной кислотой.
Эти металлы – Al, Fe, Cr, Ni и некоторые другие – при контакте с безводными кислотами сразу же покрываются продуктами окисления (пассивируются). Продукты окисления, образующие прочные пленки, могут растворяться в водных растворах кислот, но нерастворимы в кислотах концентрированных.
Это обстоятельство используют в промышленности. Например, концентрированную серную кислоту хранят и перевозят в железных бочках.
** 8.13. Напишите формулы водородных соединений пяти элементов главной подгруппы VI группы. Все они в той или иной мере являются кислотами. Исходя из закономерностей Периодической таблицы, расположите эти кислоты в ряд от самой слабой до самой сильной кислоты.
Все что необходимо знать о серной кислоте(H2SO4)
Характеристика

Основное свойство H2SO4 – гигроскопичность, поэтому её часто используют для поглощения влаги из воздуха. В течение этого процесса также происходит выделение тепла. Температура кипения зависит от степени насыщенности. При 98%-ой концентрации, достигается максимум, который составляет 330 °C, при этом возникает распад на H2O и SO3. Температура плавления – 10,38 °C, плотность – 1,84 г/см3.
Состояние жидкости влияет на то, как она изменяет другие элементы при взаимодействии с ними. Все металлы, стоящие в электрохимическом ряду активности, включая серебро, поддаются окислению при 100%-ой концентрации. Разбавленная H2SO4 окисляет все металлы, находящиеся в электрохимическом ряду активности левее водорода, однако платина и золото не состоят в этом списке.
Наблюдаются изменения при взаимодействии с органическими соединениями и неметаллами, итогом которого становится преобразование некоторых из них в уголь. H2SO4 способна растворять SO3, образуя олеум.
Классификация
H2SO4 выше 40% называется концентрированной. Она известна как сильный окислитель и при контакте с серебром или палладием растворяет их. Во время нагревания демонстрирует окислительно-восстановительные качества. Концентрация разбавленных растворов не превышает 40%. Они отличаются меньшей активностью и способны взаимодействовать с медью и латунью.
Чтобы преобразовать концентрированную смесь в разбавленную, более тяжёлую жидкость нужно смешать с H2O. Важно добавлять именно кислоту в воду, соблюдая осторожность. Если сделать наоборот, образуется кипение и токсикологические брызги.
Технологии получения

Традиционными методами, используемыми в промышленности, выступают контактный и нитрозный.
Контактный метод
Нитрозный метод
Нитрозная технология бывает двух видов: камерная и башенная. Преимущества данного подхода состоят в том, что он не требует больших денежных затрат или сложного технологичного оборудования, а также гарантирует переработку диоксида серы.
Но имеются и минусы. В конечном итоге производитель получает 75%-ую концентрацию, которая заметно уступает по качеству тому, что выходит при контактном способе. В составе наблюдается содержание оксида азота, железа и иных примесей. Возврат оксидов азота осуществляется не полностью. Нитрозный способ вреден для экологии, поскольку допускает значительные выбросы токсинов в атмосферу. Тем не менее, этот подход всё равно остаётся довольно-таки популярным.
Исходный материал – сернистый газ. Его преобразование в H2SО4 осуществляется в процессе окислительной реакции с двуокисью серы и присоединения воды. Нитрозная техника не обходится без добавления окислов азота, поскольку двуокись серы не вступает в прямой контакт с кислородом. В течение данного процесса высшие окислы азота превращаются в окись азота NO. Позднее окись азота NO снов окисляется кислородом, преобразуясь в высшие окислы.
В каких отраслях находит применение
Это далеко не все области применения. Вещество выполняет функции эмульгатора при приготовлении пищевой продукции, помогает эффективно устранять отходы в воде. Считается действительно необходимым компонентом в индустрии, замену которой трудно найти. Говоря об этом продукте, Дмитрий Менделеев отмечал, как часто к его помощи прибегают в техническом производстве, и что без него невозможно и невыгодно заниматься приготовлением других веществ.
Соли серной кислоты и область их применения
История изучения
Начало исследований было заложено ещё в Древней Греции, когда учёные заинтересовались происхождением медного купороса и его особенностями. Купорос находил применение как в медицинской практике, так и в металлургии. Первые достижения датируются XIII веком. Согласно записям алхимиков того периода для этого прибегли к нагреванию алюмокалиевых квасцов. Изучив природу квасцов, в XV веке учёные смогли приступить к следующей стадии опытов. Чуть позже, во времена Средневековья в Европе, вещество было известно как «купоросное масло», однако название было изменено на привычную современным людям “кислоту”.
Следом за Джошуа к производству приступил Джон Робак из Англии, несколько адаптировав технику. Вместо стеклянных резервуаров он взял освинцованные камеры крупного размера, поскольку они были дешевле. Нововведения Робака позволяли получить 65%-ный раствор. Приёмы англичанина сохраняли популярность в течение двухсот лет. 78%-ая концентрация появилась благодаря химикам из Англии и Франции Гловеру и Гей-Люссаку. В отличие от прошлого варианта этот оказался неподходящим для создания красителей.
Новые техники были разработаны в начале XIX века. На первых порах для этого брали азот, такой способ вскоре стал именоваться «нитрозным». Также для быстрого протекания реакции обращались к платине. Только в тридцатые годы XIX века Перегрином Филипсом был запатентован экономичный путь обработки оксида серы (VI) и концентрированного раствора. А в 1864 году был запущен выпуск природных фосфорных удобрений.
К концу 1800-х годов европейские страны наладили выпуск продукции в количестве до одного миллиона тонн, а лидирующие позиции в поставке заняли Англия и Германия. На их долю приходился 71% от общего объёма. В России корпорации подобного рода открылись после 1805 года в Москве.
Производство в России
Особенности транспортировки
При транзите следует соблюдать осторожность из-за резких ядовитых свойств продукта. Он взрывоопасен и относится к восьмому классу опасности, который включает ядовитые и коррозионные грузы. Допущение перевозчиком грубых ошибок при транспортировке, ставит под угрозу не только людей, но и экологию.
Перевозка происходит при соблюдении правил, гарантирующих безопасность населения. Требуется подобрать устойчивую ёмкость для транзита. Цистерны должны быть изготовлены из сплавов, которые не разрушатся под воздействием ядов. Для перевозки опасных токсинов подойдут сернокислотные химические резервуары. При необходимости поддерживать температуру, как с дымящейся жидкостью, подбираются цистерны-термосы. Для обычного груза подойдёт сернокислотная канистра.
Транспортировка допускается лишь на автомобилях со специальной маркировкой, предупреждающей об опасном грузе. Перевозить цистерны имеют право водители, получившие свидетельство АДР, подтверждающее их компетентность. Они не ограничены во времени при перевозке, поскольку обязаны соблюдать скоростной режим для исключения возможности попадания в аварию. Чтобы избежать ситуаций, создающих угрозу жизни населения, водитель должен ехать по специально-разработанному маршруту, исключающему места большого скопления людей и производственные объекты.
Вред для человеческого здоровья
Токсичная жидкость угрожает здоровью человека не только из-за риска попадания капель на кожные ткани, она может нанести вред внутренним органам поскольку в её состав входит не менее едкий сернистый газ. Ей характерна чрезвычайная агрессивность, а входящий в состав мышьяк усиливает признаки отравления. Безвредной дозой содержания H2SО4 в воздухе считается 0,3 мг на 1 кв. м.
Признаки отравления
Первая помощь и лечение
При контакте с серной кислотой важно в первую очередь вызвать скорую помощь. До того как приедут врачи, пострадавший может самостоятельно облегчить своё состояние. Если химический продукт попал внутрь, нужно промыть желудок тёплой водой, а затем выпить 100 г оливкового или подсолнечного масла маленькими глотками. Для большей пользы можно проглотить немного льда или выпить молока. Это поможет снизить содержание H2SО4.
Если жидкость попала на слизистую оболочку глаз, необходимо промыть их проточной водой. До прибытия скорой помощи в глаза следует закапать раствор новокаина и дикаина. При отравлении парами постращавшему требуется срочно выйти на свежий воздух и промыть слизистые оболочки водой. Чтобы уменьшить площадь повреждения тканей, обожжённый участок кожи нужно промыть проточной водой и приложить повязку с содой.
Если у больного наблюдается желудочное кровотечение, ему необходимо переливание крови и также введение плазмы. В ряде случаев при кровотечении может понадобиться хирургическое вмешательство.
Интересные факты о серной кислоте
Хотя сегодня принято изготавливать серную кислоту на специальных предприятиях, она всё же встречается в природе, причём в 100%-ом виде. Например, в Италии на острове Сицилия можно увидеть, как со дна Мёртвого моря просачивается H2SО4. Это место принято называть Озером смерти, живые существа стараются не подходить слишком близко к нему. Выделение серной кислоты со дна происходит из-за содержания в земной коре пирита.
Серная кислота может выделяться и при сильных извержениях вулкана. Такие явления достаточно опасны для людей и окружающей среды. Одними из последствий попадания H2SО4 в атмосферу могут стать климатические изменения. Серная кислота считается главной причиной, по которой выпадают кислотные дожди, а выделяется она из-за попадания в воздух диоксида серы.
Как уже было ранее замечено, серная кислота эффективно поглощает воду из воздуха. Это качество позволяет использовать её для осушения газов. Раньше было принято наливать жидкость в небольшие ёмкости и оставлять между стёклами. Это помогало предотвратить запотевание окон в комнате.
Характерные химические свойства кислот
Содержание:
Кислоты – это химические соединения, содержащие в себе положительный атом водорода (катион H+) и кислотный остаток (анион A-). Является сложным веществом.
Общая характеристика
В первую очередь кислоты различают по растворимости. Есть нерастворимые, растворимые и полурастворимые кислоты. Эти различия прописаны в таблице растворимости, так что наизусть запоминать не требуется.
Классификация:
Бескислородные кислоты – это растворы галогеноводородов, атомы которых в растворе связаны полярной ковалентной связью. Название кислоты складывается из названия кислотного остатка в первую очередь, а дальше называется катион (водород). Так с хлором и водородом образуется хлороводородная кислота, а с серой – сероводородная.
Кислородосодержащие кислоты, или оксокислоты называют за счёт наличия в них кислорода. Общего принципа построения названия этих кислот нет, так что их названия необходимо запоминать на память.
Физические свойства
Кислоты, в зависимости от условий, могут быть в трёх агрегатных состояниях: в жидком, твёрдом и газообразном состоянии. Кислоты могут обладать цветом и запахом.
Химические свойства
Изменение цвета индикаторов
Кислота в водной среде способна изменить цвет разных индикаторов. Кислоты окрашивают в красных цвет лакмус, метилоранж и универсальный индикатор. Фенолфталеин не окрашивается.
Взаимодействие кислот с металлами
Кислота способна реагировать только с металлами, находящимися левее водорода в ряду активности металлов.
Из приведенного выше химического уравнения нужно отметить, что при взаимодействии кислоты и металла происходит реакция замещения, образуется соль и выделяется H2.
Взаимодействие кислот с основными и амфотерными оксидами
При взаимодействии кислоты с основным или амфотерным оксидами происходит реакция обмена в результате которой образуются соль и H2O.
В качестве примера приведены следующие реакции:
Из приведённого выше химического уравнения нужно отметить, что в реакциях основного оксида калия и амфотерного оксида алюминия (III) с кислотами, образуется соль и H2O.
Взаимодействие кислот с основными и амфотерными гидроксидами
Из приведённой выше химического уравнения нужно отметить, что при реакции основного гидроксида калия и амфотерного гидроксида алюминия (III) с кислотами образуются соль и H2O.
Взаимодействие кислот с солями
Реакция кислоты с солью является реакцией обмена, так же ее называют реакцией нейтрализации. Она возможно только в случае выпадения соли в осадок, выделения газа, слабые электролиты или вода. Рассмотрим все случаи более подробно.
Из приведённого выше химического уравнения можно увидеть, что при взаимодействии кислоты и соли образуются новые кислота и нерастворимая соль, которые выпадают в осадок. Осадок может иметь различную окраску, плотность и консистенцию.
Из приведённых выше химических уравнений нужно отметить, что при реакции соли с кислотой образуется новая соль и выделяется газ. Разберём одну из реакций: при взаимодействии твёрдого хлорида натрия с концентрированной хлороводородной кислотой образовалась натриевая соль серной кислоты и выделился летучий газ хлороводород.
Такие реакции возможны только при условии, когда одним из реагентов сильный электролит. Для того, чтобы убедиться, что реакция будет протекать используют вытеснительный ряд:
В этом ряду кислоты расположены так, что в растворах кислот и их солей могут в результате реакции вытесняют из раствора те, что стоят левее в ряду. Азотная и фосфорная кислоты находятся на одном месте в ряду, т.к. имеют одинаковые вытеснительные способности.
Из приведённого выше химического уравнения нужно отметить, что хлороводородная кислота, которая находится в данном ряду левее, способна вытеснять кислотный остаток карбоновой кислоты, стоящей в ряду правее. Нужно учитывать, что карбоновая кислота слабая и при стандартных условиях она распадется на углекислый газ и воду. Углекислый газ выделяется из раствора, а вода остаётся.
Разложение кислородсодержащих кислот
В результате реакции разложения кислородсодержащих кислот всегда образуется вода и оксид.
Из приведённых выше реакций можно увидеть, что карбоновая легко разлагается при обычных условиях, так как является одной из самых слабой кислотой. Для разложения сернистой и кремниевой кислоты их растворы необходимо нагреть. Во всех трёх реакция в результате образуется вода и оксиды кислотных остатков.
концентрированная кислота
Тематики
Смотреть что такое “концентрированная кислота” в других словарях:
КИСЛОТА УКСУСНАЯ — Acidum aceticum. Свойства. Кислота уксусная официнальна в трех концентрациях: а) концентрированная ледяная) уксусная кислота, содержащая 96 100 % кислоты. Это бесцветная, прозрачная, летучая жидкость, застывающая при температуре ниже 0°С, смешив … Отечественные ветеринарные препараты
СОЛЯНАЯ КИСЛОТА — (НСl), водный раствор хлороводорода, бесцветного газа с резким запахом. Получают действием серной кислоты на поваренную соль, как побочный продукт хлорирования углеводородов, или реакцией водорода и хлора. Соляная кислота используется, для… … Научно-технический энциклопедический словарь
Серная кислота — H2SO4, сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях тяжёлая маслянистая жидкость без цвета и запаха. В технике С. к. называют её смеси как с водой, так и с серным ангидридом. Если… … Большая советская энциклопедия
Азотная кислота — Эта статья включает описание термина «Меланж»; см. также другие значения. Азотная кислота … Википедия
Серная кислота — Серная кислота … Википедия
серная кислота — H2SO4, сильная двухосновная кислота. Безводная серная кислота бесцветная маслянистая жидкость, плотность 1,8305 г/см3, tпл 10,3°C, tкип 279,6°C. С водой смешивается во всех отношениях. Концентрированная серная кислота реагирует почти со всеми… … Энциклопедический словарь
УКСУСНАЯ КИСЛОТА — Acidum aceticum. Свойства. СН3СООН. Выпускается в трех концентрациях: концентрированная (ледяная) уксусная кислота, содержащая 96 100 % СН3СООН; бесцветная прозрачная летучая жидкость сильно кислого запаха и вкуса, смешивающаяся во всех отношени … Отечественные ветеринарные препараты
Уксусная кислота — Уксусная кислота … Википедия
ГОСТ 667-73: Кислота серная аккумуляторная. Технические условия — Терминология ГОСТ 667 73: Кислота серная аккумуляторная. Технические условия оригинал документа: 3.12. Определение массовой доли веществ, восстанавливающих марганцовокислый калий Метод основан натитровании пробы серной кислоты раствором… … Словарь-справочник терминов нормативно-технической документации
Молочная кислота — Молочная кислота … Википедия
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.
В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.
При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
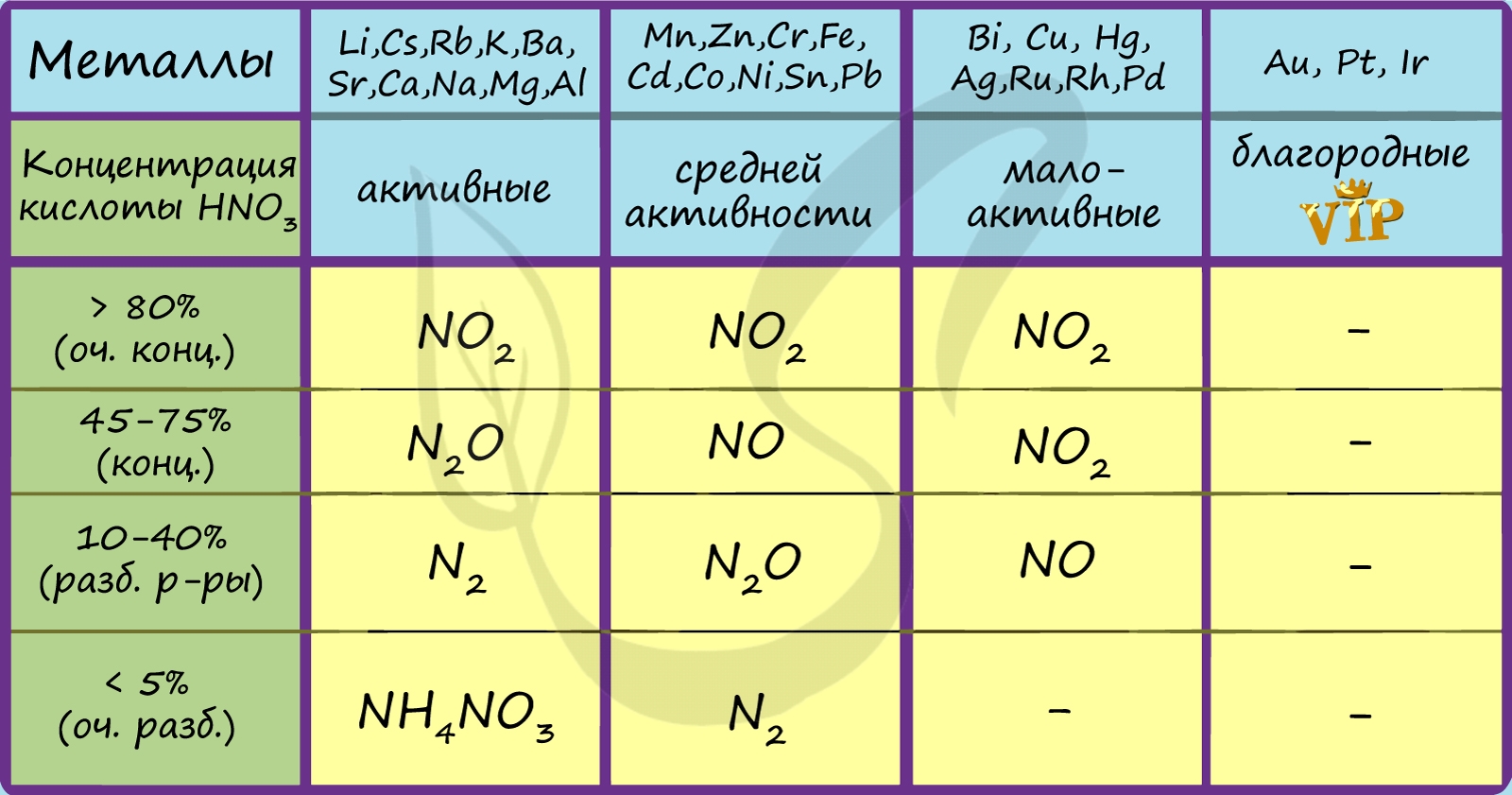
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.
Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.
Нитрат аммония получают реакция аммиака с азотной кислотой.
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
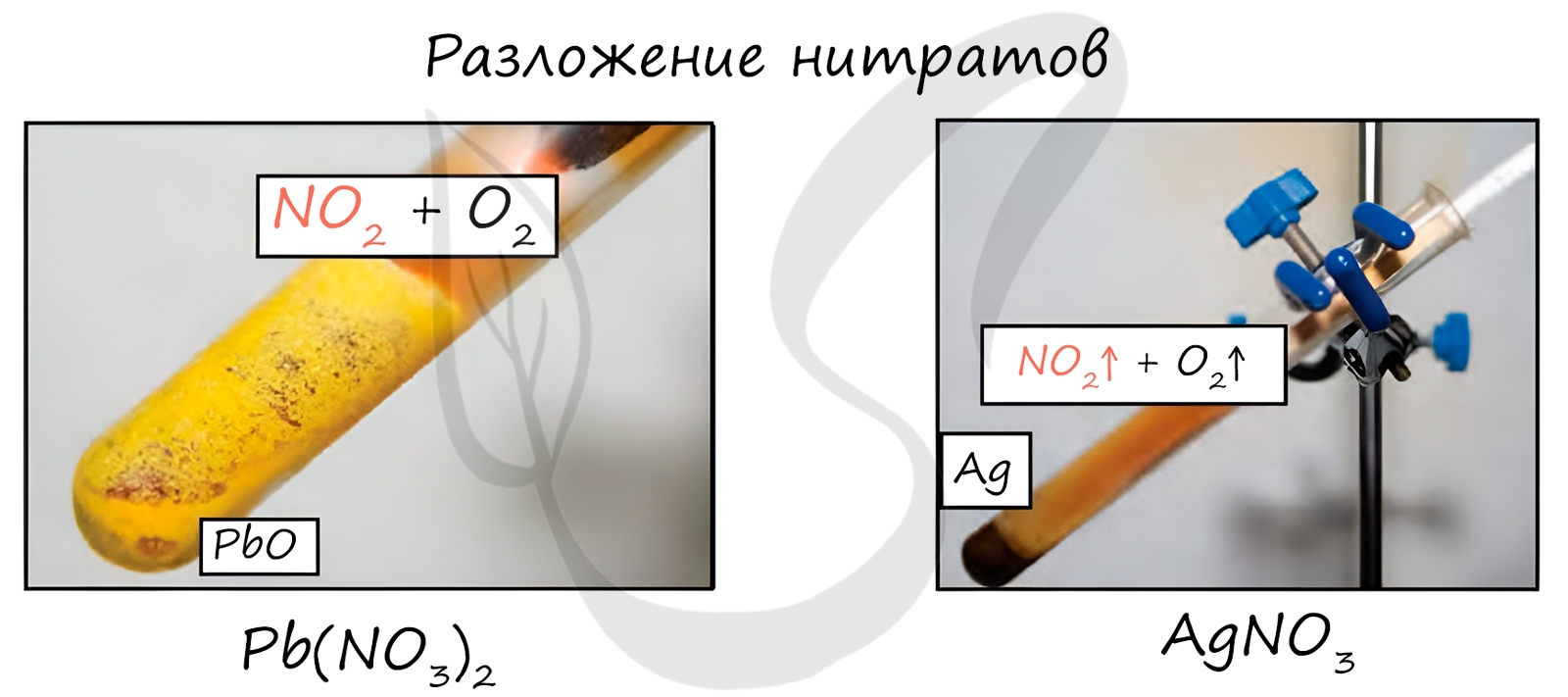
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.