какая кислота соответствует оксиду so3
Кислотные оксиды

Всего получено оценок: 1195.
Всего получено оценок: 1195.
Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород. В названиях оксидов сначала указывают слово оксид, затем название второго элемента, которым он образован. Какие особенности имеют кислотные оксиды, и чем они отличаются от других видов оксидов?
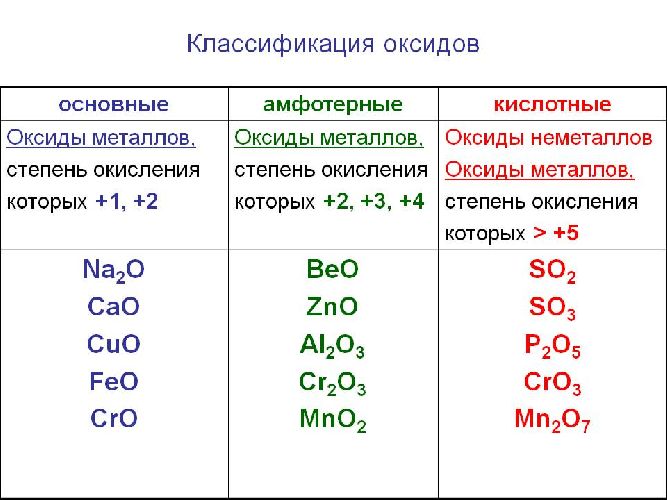
Классификация оксидов
Оксиды делятся на солеобразующие и несолеобразующие. Уже по названию ясно, что несолеобразующие не образуют солей. Таких оксидов немного : это вода H2 O, фторид кислорода OF2 (если условно его считать оксидом), угарный газ, или оксид углерода (II), монооксид углерода CO; оксиды азота (I) и (II): N2 O (оксид диазота, веселящий газ) и NO (монооксид азота).
Солеобразующие оксиды образуют соли при взаимодействии с кислотами или щелочами. В качестве гидроксидов им соответствуют основания, амфотерные основания и кислородосодержащие кислоты. Соответственно они называются основными оксидами (например, CaO), амфотерными оксидами (Al2 O3 ) и кислотными оксидами, или ангидридами кислот (CO2).
Основные свойства кислотных оксидов
Типичными реакциями являются взаимодействие кислотных оксидов с основаниями в результате чего образуется соль и вода:
Все кислотные оксиды, кроме диоксида кремния SiO2 (кремниевый ангидрид, кремнезем), реагируют с водой, образуя кислоты:
Кислотные оксиды образуются при взаимодействии с кислородом простых и сложных веществ (S+O2 =SO2 ), либо при разложении в результате нагревания сложных веществ, содержащих кислород, – кислот, нерастворимых оснований, солей (H2 SiO3 =SiO2 +H2 O).
Список кислотных оксидов:
| Название кислотного оксида | Формула кислотного оксида | Свойства кислотного оксида |
| Оксид серы (IV) | SO2 | бесцветный токсичный газ с резким запахом |
| Оксид серы (VI) | SO3 | легколетучая безцветная токсичная жидкость |
| Оксид углерода (IV) | CO2 | бесцветный газ без запаха |
| Оксид кремния (IV) | SiO2 | бесцветные кристаллы, обладающие прочностью |
| Оксид фосфора (V) | P2 O5 | белый легковозгораемый порошок с неприятным запахом |
| Оксид азота (V) | N2 O5 | вещество, состоящее из бесцветных летучих кристаллов |
| Оксид хлора (VII) | Cl2 O7 | бесцветная маслянистая токсичная жидкость |
| Оксид марганца (VII) | Mn2 O7 | жидкость с металлическим блеском, являющаяся сильным окислителем. |
Что мы узнали?
Кислотные оксиды относятся к солеобразующим оксидам и образуются с помощью кислот. Кислотные оксиды вступают в реакции с основаниями и водой, а их образование происходит при нагревании и разложении сложных веществ.
Какая кислота соответствует оксиду so3
§8.2 Оксиды и их классификация.
Как мы уже знаем, оксиды бывают кислотные и основные. Это деление положено в основу их классификации.
Большинство кислотных оксидов хорошо реагирует с водой, давая кислоту. Например, кислый вкус простой газированной воды объясняется образованием угольной кислоты Н 2 СО 3 из кислотного оксида СО 2 :
СО 2 + Н 2 О = Н 2 СО 3 (угольная кислота)
В простейших случаях формулу образующейся кислоты легко получить из формулы кислотного оксида простым сложением. Например:
кислотный оксид (не растворим в воде)
соль кремниевой кислоты H 2 SiO 3
Полученную соль кремниевой кислоты можно превратить в саму кремниевую кислоту добавлением другой кислоты:
Na 2 SiO 3 + 2 HCl = H 2 SiO 3 + 2 NaCl
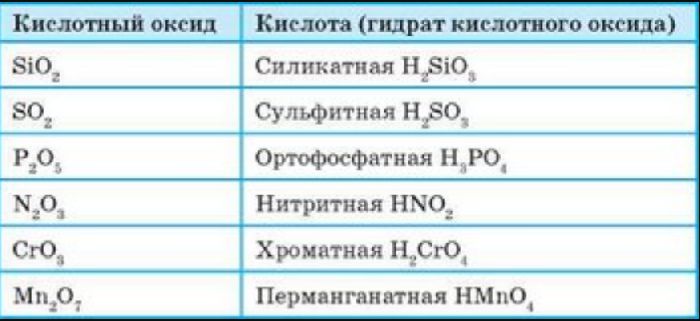
Таким образом, кислотному оксиду всегда соответствует определенная кислота :
CO 2 (оксид углерода) – H 2 CO 3 (угольная кислота) ;
SO 3 (оксид серы VI) – H 2 SO 4 ( серная кислота) ;
SiO 2 (оксид кремния) – H 2 SiO 3 ( кремниевая кислота).
Поскольку реакция с основаниями является общей для всех кислотных оксидов, им можно дать такое определение:
Оксиды, которые взаимодействуют с основаниями с образованием соли и воды, называются КИСЛОТНЫМИ ОКСИДАМИ.
** Кислотные оксиды, как мы видим, образованы в основном неметаллами. Вам следует запомнить только два оксида металлов, которые также являются кислотными. Это оксиды хрома и марганца, в которых металлы имеют НАИБОЛЬШУЮ из всех возможных степень окисления:
CrO 3 (оксид хрома VI) – H 2 CrO 4 (хромовая кислота) ;
Mn 2 O 7 (оксид марганца VII) – HMnO 4 (марганцовая кислота).
Осн о вные оксиды образуются только металлами. Некоторые из них легко реагируют с водой, давая соответствующее основание:
Li 2 O + H 2 O = 2 LiOH (основание – гидроксид лития).
Еще один пример – хорошо известная нам реакция получения гашеной извести из оксида кальция и воды.
CaO + H 2 O = Ca(OH) 2 (основание – гидроксид кальция).
Существует, однако большое количество нерастворимых основных оксидов. Их относят именно к основным оксидам благодаря реакциям с кислотами :
ZnO + H 2 O = реакция не идет (ZnO не растворим в воде);
ZnO + 2 HCl = ZnCl 2 (соль) + H 2 O
[ZnO + H 2 O] = Zn(OH) 2
Zn(OH) 2 + 2 HCl = ZnCl 2 (соль) + H 2 O
Каждому основному оксиду соответствует определенное основание:
MgO (оксид магния) – Mg(OH) 2 (гидроксид магния);
Fe 2 O 3 (оксид железа III) – Fe(OH) 3 (гидроксид железа III);
Na 2 O (оксид натрия) – NaOH (гидроксид натрия).
Таким образом, общее свойство основных оксидов заключается в способности реагировать с кислотами с образованием соли и воды.
Оксиды, которые взаимодействуют с КИСЛОТАМИ с образованием соли и воды, называются ОСНОВНЫМИ ОКСИДАМИ.
** Оксиды хрома и марганца, в которых металл имеет низшую степень окисления, являются обыкновенными основными оксидами (как и оксиды всех остальных металлов). Вот какие гидроксиды им соответствуют:
CrO (оксид хрома II) – Cr(OH) 2 (гидроксид хрома II);
MnO (оксид марганца II) – Mn(OH) 2 ( гидроксид марганца II).
Соединения хрома (II) крайне неустойчивы и быстро переходят в соединения хрома (III). С применением многих интересных оксидов мы уже познакомились в главе 6 “кислород”.
8.6. Исходя из Периодической таблицы, напишите формулы оксидов следующих элементов: калия, бария, железа (II), хрома (III), хлора (VII), кремния (IV). Подчеркните формулы кислотных оксидов.
** 8.7. Исходя из Периодической таблицы, напишите формулы оксидов следующих элементов: германия Ge (одну формулу), селена Se (две формулы), фосфора P (две формулы), бора B (одну формулу), бериллия Be (одну формулу).
8.8. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca → CaO → Ca(OH) 2 → CaSO 4
S → SO 2 → SO 3 → H 2 SO 4 → CaSO 4
8.9. Какой объем газообразного оксида серы (VI) при н.у. потребуется для нейтрализации раствора, получившегося при растворении 56 г CaO в воде?
Классификация неорганических веществ
Среди простых веществ выделяют металлы и неметаллы. Среди сложных: оксиды, основания, кислоты и соли. Классификация неорганических веществ построена следующим образом:
Большинство химических свойств мы изучим по мере продвижения по периодической таблице Д.И. Менделеева. В этой статье мне хотелось бы подчеркнуть ряд принципиальных деталей, которые помогут в дальнейшем при изучении химии.
Оксиды
Все оксиды подразделяются на солеобразующие и несолеобразующие. Солеобразующие имеют соответствующие им основания и кислоты (в той же степени окисления (СО)!) и охотно вступают в реакции солеобразования. К ним относятся, например:
Солеобразующие оксиды, в свою очередь, делятся на основные, амфотерные и кислотные.
Основным оксидам соответствуют основания в той же СО. В химических реакциях основные оксиды проявляют основные свойства, образуются исключительно металлами. Примеры: Li2O, Na2O, K2O, Rb2O CaO, FeO, CrO, MnO.
Основные оксиды взаимодействуют с водой с образованием соответствующего основания (реакцию идет, если основание растворимо) и с кислотными оксидами и кислотами с образованием солей. Между собой основные оксиды не взаимодействуют.
Li2O + H2O → LiOH (основный оксид + вода → основание)
Здесь не происходит окисления/восстановления, поэтому сохраняйте исходные степени окисления атомов.
Эти оксиды действительно имеют двойственный характер: они проявляют как кислотные, так и основные свойства. Примеры: BeO, ZnO, Al2O3, Fe2O3, Cr2O3, MnO2, PbO, PbO2, Ga2O3.
С водой они не взаимодействуют, так как продукт реакции, основание, получается нерастворимым. Амфотерные оксиды реагируют как с кислотами и кислотными оксидами, так и с основаниями и основными оксидами.
ZnO + KOH + H2O → K2[Zn(OH)4] (амф. оксид + основание = комплексная соль)
ZnO + N2O5 → Zn(NO3)2 (амф. оксид + кисл. оксид = соль; СО азота сохраняется в ходе реакции)
Fe2O3 + HCl → FeCl3 + H2O (амф. оксид + кислота = соль + вода; обратите внимание на то, что СО Fe = +3 не меняется в ходе реакции)
Проявляют в ходе химических реакций кислотные свойства. Образованы металлами и неметаллами, чаще всего в высокой СО. Примеры: SO2, SO3, P2O5, N2O3, NO2, N2O5, SiO2, MnO3, Mn2O7.
Кислотные оксиды вступают в реакцию с основными и амфотерными, реагируют с основаниями. Реакции между кислотными оксидами не характерны.
SO2 + Na2O → Na2SO3 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +4)
SO3 + Li2O → Li2SO4 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +6)
P2O5 + NaOH → Na3PO4 + H2O (кисл. оксид + основание = соль + вода)
Реакции несолеобразующих оксидов с основаниями, кислотами и солеобразующими оксидов редки и не приводят к образованию солей. Некоторые из несолеобразующих оксидов используют в качестве восстановителей:
FeO + CO → Fe + CO2 (восстановление железа из его оксида)
Основания
Основания классифицируются по количеству гидроксид-ионов в молекуле на одно-, двух- и трехкислотные.
Так же, как и оксиды, основания различаются по свойствам. Все основания хорошо реагируют с кислотами, даже нерастворимые основания способны растворяться в кислотах. Также нерастворимые основания при нагревании легко разлагаются на воду и соответствующий оксид.
Mg(OH)2 → (t) MgO + H2O (при нагревании нерастворимые основания легко разлагаются)
Если в ходе реакции основания с солью выделяется газ, выпадает осадок или образуется слабый электролит (вода), то такая реакция идет. Нерастворимые основания с солями почти не реагируют.
Ba(OH)2 + NH4Cl → BaCl2 + NH3 + H2O (в ходе реакции образуется нестойкое основание NH4OH, которое распадается на NH3 и H2O)
KOH + BaCl2 ↛ реакция не идет, так как в продуктах нет газа/осадка/слабого электролита (воды)
В растворах щелочей pH > 7, поэтому лакмус окрашивает их в синий цвет.
Al(OH)3 + HCl → AlCl3 + H2O (амф. гидроксид + кислота = соль + вода)
Al(OH)3 + KOH → K[Al(OH)4] (амф. гидроксид + основание = комплексная соль)
При нагревании до высоких температур комплексные соли не образуются.
Кислоты
Кислоты отлично реагируют с основными оксидами, основаниями, растворяя даже те, которые выпали в осадок (реакция нейтрализации). Также кислоты способны вступать в реакцию с теми металлами, которые стоят в ряду напряжений до водорода (то есть способны вытеснить его из кислоты).
Zn + HCl → ZnCl2 + H2↑ (реакция идет, так как цинк стоил в ряду активности левее водорода и способен вытеснить его из кислоты)
Cu + HCl ↛ (реакция не идет, так как медь расположена в ряду активности правее водорода, менее активна и не способна вытеснить его из кислоты)
Все кислоты подразделяются на сильные и слабые. Напомню, что мы составили подробную таблицу сильных и слабых кислот (и оснований!) в теме гидролиз. В реакции из сильной кислоты (соляной) можно получить более слабую, например, сероводородную или угольную кислоту.
В завершении подтемы кислот предлагаю вам вспомнить названия основных кислот и их кислотных остатков.
Блиц-опрос по теме Классификация неорганических веществ
2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
Прежде чем начать говорить про химические свойства оксидов, нужно вспомнить о том, что все оксиды делятся на 4 типа, а именно основные, кислотные, амфотерные и несолеобразующие. Для того чтобы определить тип какого-либо оксида, прежде всего нужно понять — оксид металла или неметалла перед вами, а затем воспользоваться алгоритмом (его надо выучить!), представленным в следующей таблице:
| Оксид неметалла | Оксид металла |
| 1) Степень окисления неметалла +1 или +2 Вывод: оксид несолеобразующий Исключение: Cl2O не относится к несолеобразующим оксидам | 1) Степень окисления металла +1 или +2 Вывод: оксид металла — основный Исключение: BeO, ZnO и PbO не относятся к основным оксидам |
| 2) Степень окисления больше либо равна +3 Вывод: оксид кислотный Исключение: Cl2O относится к кислотным оксидам, несмотря на степень окисления хлора +1 | 2) Степень окисления металла +3 или +4 Вывод: оксид амфотерный Исключение: BeO, ZnO и PbO амфотерны, несмотря на степень окисления +2 у металлов 3) Степень окисления металла +5, +6, +7 Вывод: оксид кислотный |
Помимо типов оксидов, указанных выше, введем также еще два подтипа основных оксидов, исходя из их химической активности, а именно активные основные оксиды и малоактивные основные оксиды.
Логично предположить, что активные основные оксиды часто вступают в те реакции, в которые не вступают малоактивные.
Следует отметить, что несмотря на то что фактически вода является оксидом неметалла (H2O), обычно ее свойства рассматривают в отрыве от свойств иных оксидов. Обусловлено это ее специфически огромным распространением в окружающем нас мире, в связи с чем в большинстве случаев вода является не реагентом, а средой, в которой может осуществляться бесчисленное множество химических реакций. Однако нередко она принимает и непосредственное участие в различных превращениях, в частности, некоторые группы оксидов с ней реагируют.
Какие оксиды реагируют с водой?
Из всех оксидов с водой реагируют только:
1) все активные основные оксиды (оксиды ЩМ и ЩЗМ);
2) все кислотные оксиды, кроме диоксида кремния (SiO2);
т.е. из вышесказанного следует, что с водой точно не реагируют:
1) все малоактивные основные оксиды;
2) все амфотерные оксиды;
3) несолеобразующие оксиды (NO, N2O, CO, SiO).
Оксид магния медленно реагирует с водой при кипячении. Без сильного нагревания реакция MgO с H2O не протекает.
Способность определить то, какие оксиды могут реагировать с водой даже без умения писать соответствующие уравнения реакций, уже позволяет получить баллы за некоторые вопросы тестовой части ЕГЭ.
Теперь давайте разберемся, как же все-таки те или иные оксиды реагируют с водой, т.е. научимся писать соответствующие уравнения реакций.
Активные основные оксиды, реагируя с водой, образуют соответствующие им гидроксиды. Напомним, что соответствующим оксиду металла является такой гидроксид, который содержит металл в той же степени окисления, что и оксид. Так, например, при реакции с водой активных основных оксидов K +1 2O и Ba +2 O образуются соответствующие им гидроксиды K +1 OH и Ba +2 (OH)2:
K2O + H2O = 2KOH – гидроксид калия
BaO + H2O = Ba(OH)2 – гидроксид бария
Все гидроксиды, соответствующие активным основным оксидам (оксидам ЩМ и ЩЗМ), относятся к щелочам. Щелочами называют все хорошо растворимые в воде гидроксиды металлов, а также малорастворимый гидроксид кальция Ca(OH)2 (как исключение).
Взаимодействие кислотных оксидов с водой так же, как и реакция активных основных оксидов с водой, приводит к образованию соответствующих гидроксидов. Только в случае кислотных оксидов им соответствуют не основные, а кислотные гидроксиды, чаще называемые кислородсодержащими кислотами. Напомним, что соответствующей кислотному оксиду является такая кислородсодержащая кислота, которая содержит кислотообразующий элемент в той же степени окисления, что и в оксиде.
Таким образом, если мы, например, хотим записать уравнение взаимодействия кислотного оксида SO3 с водой, прежде всего мы должны вспомнить основные, изучаемые в рамках школьной программы, серосодержащие кислоты. Таковыми являются сероводородная H2S, сернистая H2SO3 и серная H2SO4 кислоты. Cероводородная кислота H2S, как легко заметить, не является кислородсодержащей, поэтому ее образование при взаимодействии SO3 с водой можно сразу исключить. Из кислот H2SO3 и H2SO4 серу в степени окисления +6, как в оксиде SO3, содержит только серная кислота H2SO4. Поэтому именно она и будет образовываться в реакции SO3 с водой:
Аналогично оксид N2O5, содержащий азот в степени окисления +5, реагируя с водой, образует азотную кислоту HNO3, но ни в коем случае не азотистую HNO2, поскольку в азотной кислоте степень окисления азота, как и в N2O5, равна +5, а в азотистой — +3:
Исключение:
Оксид азота (IV) (NO2) является оксидом неметалла в степени окисления +4, т.е. в соответствии с алгоритмом, описанным в таблице в самом начале данной главы, его нужно отнести к кислотным оксидам. Однако не существует такой кислоты, которая содержала бы азот в степени окисления +4.
В случае оксида NO2 принято считать, что ему соответствуют сразу две кислоты, поскольку его взаимодействие с водой приводит к одновременному образованию двух кислот:
Взаимодействие оксидов друг с другом
Прежде всего нужно четко усвоить тот факт, что среди солеобразующих оксидов (кислотных, основных, амфотерных) практически никогда не протекают реакции между оксидами одного класса, т.е. в подавляющем большинстве случаев невозможно взаимодействие:
1) основный оксид + основный оксид ≠
2) кислотный оксид + кислотный оксид ≠
3) амфотерный оксид + амфотерный оксид ≠
В то время, как практически всегда возможно взаимодействие между оксидами, относящимися к разным типам, т.е. практически всегда протекают реакции между:
1) основным оксидом и кислотным оксидом;
2) амфотерным оксидом и кислотным оксидом;
3) амфотерным оксидом и основным оксидом.
В результате всех таких взаимодействий всегда продуктом является средняя (нормальная) соль.
Рассмотрим все указанные пары взаимодействий более детально.
В результате взаимодействия:
MexOy + кислотный оксид, где MexOy – оксид металла (основный или амфотерный)
образуется соль, состоящая из катиона металла Me (из исходного MexOy) и кислотного остатка кислоты, соответствующей кислотному оксиду.
Для примера попробуем записать уравнения взаимодействия следующих пар реагентов:
В первой паре реагентов мы видим основный оксид (Na2O) и кислотный оксид (P2O5). Во второй – амфотерный оксид (Al2O3) и кислотный оксид (SO3).
Как уже было сказано, в результате взаимодействия основного/амфотерного оксида с кислотным образуется соль, состоящая из катиона металла (из исходного основного/амфотерного оксида) и кислотного остатка кислоты, соответствующей исходному кислотному оксиду.
Попробуем записать в качестве примера уравнения взаимодействия
ZnO + Na2O и Al2O3 + BaO
Как мы уже писали выше, практически всегда протекает реакция:
MexOy + кислотный оксид,
где MexOy – либо основный, либо амфотерный оксид металла.
Однако следует запомнить два «привередливых» кислотных оксида – углекислый газ (CO2) и сернистый газ (SO2). «Привередливость» их заключается в том, что несмотря на явные кислотные свойства, активности CO2 и SO2 недостаточно для их взаимодействия с малоактивными основными и амфотерными оксидами. Из оксидов металлов они реагируют только с активными основными оксидами (оксидами ЩМ и ЩЗМ). Так, например, Na2O и BaO, являясь активными основными оксидами, могут с ними реагировать:
В то время, как оксиды CuO и Al2O3, не относящиеся к активным основным оксидам, в реакцию с CO2 и SO2 не вступают:
CO2 + CuO ≠
SO2 + CuO ≠
Взаимодействие оксидов с кислотами
С кислотами реагируют основные и амфотерные оксиды. При этом образуются соли и вода:
Несолеобразующие оксиды не реагируют с кислотами вообще, а кислотные оксиды не реагируют с кислотами в большинстве случаев.
Когда все-таки кислотный оксид реагирует с кислотой?
Решая часть ЕГЭ с вариантами ответа, вы должны условно считать, что кислотные оксиды не реагируют ни с кислотными оксидами, ни с кислотами, за исключением следующих случаев:
1) диоксид кремния, будучи кислотным оксидом, реагирует с плавиковой кислотой, растворяясь в ней. В частности, благодаря этой реакции в плавиковой кислоте можно растворить стекло. В случае избытка HF уравнение реакции имеет вид:
а в случае недостатка HF:
2) SO2, будучи кислотным оксидом, легко реагирует с сероводородной кислотой H2S по типу сопропорционирования:
3) Оксид фосфора (III) P2O3 может реагировать с кислотами-окислителями, к которым относятся концентрированная серная кислота и азотная кислота любой концентрации. При этом степень окисления фосфора повышается от значения +3 до +5:
| P2O3 | + | 2H2SO4 | + | H2O | =t o => | 2SO2 | + | 2H3PO4 |
| (конц.) |
| 3P2O3 | + | 4HNO3 | + | 7H2O | =t o => | 4NO↑ | + | 6H3PO4 |
| (разб.) |
| P2O3 | + | 4HNO3 | + | H2O | =t o => | 2H3PO4 | + | 4NO2↑ |
| (конц.) |
4) Оксид серы (IV) SO2 может быть окислен азотной кислотой, взятой в любой концентрации. При этом степень окисления серы повышается с +4 до +6.
| 2HNO3 | + | SO2 | =t o => | H2SO4 | + | 2NO2↑ |
| (конц.) |
| 2HNO3 | + | 3SO2 | + | 2H2O | =t o => | 3H2SO4 | + | 2NO↑ |
| (разб.) |
Взаимодействие оксидов с гидроксидами металлов
С гидроксидами металлов как основными, так и амфотерными реагируют кислотные оксиды. При этом образуется соль, состоящая из катиона металла (из исходного гидроксида металла) и кислотного остатка кислоты, соответствующей кислотному оксиду.
Кислотные оксиды, которым соответствуют многоосновные кислоты, с щелочами могут образовывать как нормальные, так и кислые соли:
CO2 + NaOH = NaHCO3
«Привередливые» оксиды CO2 и SO2, активности которых, как уже было сказано, не хватает для протекания их реакции с малоактивными основными и амфотерными оксидами, тем не менее, реагируют с большей частью соответствующих им гидроксидов металлов. Точнее, углекислый и сернистый газы взаимодействуют с нерастворимыми гидроксидами в виде их суспензии в воде. При этом образуются только основные соли, называемые гидроксокарбонатами и гидроксосульфитами, а образование средних (нормальных) солей невозможно:
Однако с гидроксидами металлов в степени окисления +3, например, такими, как Al(OH)3, Cr(OH)3 и т.д., углекислый и сернистый газ не реагируют вовсе.
Следует отметить также особую инертность диоксида кремния (SiO2), в природе наиболее часто встречаемого в виде обычного песка. Данный оксид является кислотным, однако из гидроксидов металлов способен реагировать только с концентрированными (50-60%) растворами щелочей, а также с чистыми (твердыми) щелочами при сплавлении. При этом образуются силикаты:
Амфотерные оксиды из гидроксидов металлов реагируют только со щелочами (гидроксидами щелочных и щелочноземельных металлов). При этом при проведении реакции в водных растворах образуются растворимые комплексные соли:
ZnO + 2NaOH + H2O = Na2[Zn(OH)4] — тетрагидроксоцинкат натрия
BeO + 2NaOH + H2O = Na2[Be(OH)4] — тетрагидроксобериллат натрия
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4] — тетрагидроксоалюминат натрия
Следует отметить, что соли, получаемые сплавлением амфотерных оксидов с твердыми щелочами, могут быть легко получены из растворов соответствующих комплексных солей их упариванием и последующим прокаливанием:
Взаимодействие оксидов со средними солями
Чаще всего средние соли с оксидами не реагируют.
Однако следует выучить следующие исключения из данного правила, часто встречающиеся на экзамене.
Одним из таких исключений является то, что амфотерные оксиды, а также диоксид кремния (SiO2) при их сплавлении с сульфитами и карбонатами вытесняют из последних сернистый (SO2) и углекислый (CO2) газы соответственно. Например:
Также к реакциям оксидов с солями можно условно отнести взаимодействие сернистого и углекислого газов с водными растворами или взвесями соответствующих солей — сульфитов и карбонатов, приводящее к образованию кислых солей:
Также сернистый газ при пропускании его через водные растворы или взвеси карбонатов вытесняет из них углекислый газ благодаря тому, что сернистая кислота является более сильной и устойчивой кислотой, чем угольная:
ОВР с участием оксидов
Восстановление оксидов металлов и неметаллов
Аналогично тому, как металлы могут реагировать с растворами солей менее активных металлов, вытесняя последние в свободном виде, оксиды металлов при нагревании также способны реагировать с более активными металлами.
Напомним, что сравнить активность металлов можно либо используя ряд активности металлов, либо, если одного или сразу двух металлов нет в ряду активности, по их положению относительно друг друга в таблице Менделеева: чем ниже и левее металл, тем он более активен. Также полезно помнить, что любой металл из семейства ЩМ и ЩЗМ будет всегда активнее металла, не являющегося представителем ЩМ или ЩЗМ.
В частности, на взаимодействии металла с оксидом менее активного металла основан метод алюмотермии, используемый в промышленности для получения таких трудновосстанавливаемых металлов, как хром и ванадий:
При протекании процесса алюмотермии образуется колоссальное количество тепла, а температура реакционной смеси может достигать более 2000 o C.
Также оксиды практически всех металлов, находящихся в ряду активности правее алюминия, могут быть восстановлены до свободных металлов водородом (H2), углеродом (C) и угарным газом (CO) при нагревании. Например:
CuO + C =t o => Cu + CO
Следует отметить, что в случае, если металл может иметь несколько степеней окисления, при недостатке используемого восстановителя возможно также неполное восстановление оксидов. Например:
Оксиды активных металлов (щелочных, щелочноземельных, магния и алюминия) с водородом и угарным газом не реагируют.
Однако оксиды активных металлов реагируют с углеродом, но иначе, чем оксиды менее активных металлов.
В рамках программы ЕГЭ, чтобы не путаться, следует считать, что в результате реакции оксидов активных металлов (до Al включительно) с углеродом образование свободного ЩМ, ЩЗМ, Mg, а также Al невозможно. В таких случаях происходит образование карбида металла и угарного газа. Например:
CaO + 3C =t o => CaC2 + CO
Оксиды неметаллов нередко могут быть восстановлены металлами до свободных неметаллов. Так, например, оксиды углерода и кремния при нагревании реагируют с щелочными, щелочноземельными металлами и магнием:
CO2 + 2Mg =t o => 2MgO + C
SiO2 + 2Mg =t o => Si + 2MgO
При избытке магния последнее взаимодействие может приводить также к образованию силицида магния Mg2Si:
SiO2 + 4Mg =t o => Mg2Si + 2MgO
Оксиды азота могут быть относительно легко восстановлены даже менее активными металлами, например, цинком или медью:
Zn + 2NO =t o => ZnO + N2
Взаимодействие оксидов с кислородом
Для того чтобы в заданиях реального ЕГЭ суметь ответить на вопрос, реагирует ли какой-либо оксид с кислородом (O2), прежде всего нужно запомнить, что оксиды, способные реагировать с кислородом (из тех, что могут попасться вам на самом экзамене) могут образовать только химические элементы из списка:
углерод С, кремний Si, фосфор P, сера S, медь Cu, марганец Mn, железо Fe, хром Cr, азот N
Встречающиеся в реальном ЕГЭ оксиды любых других химических элементов с кислородом реагировать не будут (!).
Для более наглядного удобного запоминания перечисленных выше списка элементов, на мой взгляд, удобна следующая иллюстрация:
Все химические элементы, способные образовывать оксиды, реагирующие с кислородом (из встречающегося на экзамене)
В первую очередь, среди перечисленных элементов следует рассмотреть азот N, т.к. отношение его оксидов к кислороду заметно отличается от оксидов остальных элементов приведенного выше списка.
Следует четко запомнить тот факт, что всего азот способен образовать пять оксидов, а именно:
Из всех оксидов азота с кислородом может реагировать только NO. Данная реакция протекает очень легко при смешении NO как с чистым кислородом, так и с воздухом. При этом наблюдается быстрое изменение окраски газа с бесцветной (NO) на бурую (NO2):
| 2NO | + | O2 | = | 2NO2 |
| бесцветный | бурый |
Для того чтобы дать ответ на вопрос — реагирует ли с кислородом какой-либо оксид любого другого из перечисленных выше химических элементов (т.е. С, Si, P, S, Cu, Mn, Fe, Cr) — прежде всего обязательно нужно запомнить их основные степени окисления (СО). Вот они:
| элемент | С | Si | P | S | Cu | Cr | Mn | Fe |
| его основные положительные СО | +2, +4 | +2, +4 | +3, +5 | +4, +6 | +1, +2 | +2, +3, +6 | +2, +4, +6, +7 | +2, +3, +6 |
Далее нужно запомнить тот факт, что из возможных оксидов указанных выше химических элементов, с кислородом будут реагировать только те, которые содержат элемент в минимальной, среди указанных выше, степени окисления. При этом степень окисления элемента повышается до ближайшего положительного значения из возможных:
Отношение его оксидов к кислороду
Минимальная среди основных положительных степеней окисления углерода равна +2, а ближайшая к ней положительная — +4. Таким образом, с кислородом из оксидов C +2 O и C +4 O2 реагирует только CO. При этом протекает реакция:
2C +2 O + O2 =t o => 2C +4 O2
CO2 + O2 ≠ — реакция невозможна в принципе, т.к. +4 – высшая степень окисления углерода.
Минимальная среди основных положительных степеней окисления кремния равна +2, а ближайшая к ней положительная — +4. Таким образом, с кислородом из оксидов Si +2 O и Si +4 O2 реагирует только SiO. Из-за некоторых особенностей оксидов SiO и SiO2 возможно окисление лишь части атомов кремния в оксиде Si +2 O. Т.е. в результате его взаимодействия с кислородом, образуется смешанный оксид, содержащий как кремний в степени окисления +2, так и кремний в степени окисления +4, а именно Si2O3 (Si +2 O·Si +4 O2):
SiO2 + O2 ≠ — реакция невозможна в принципе, т.к. +4 – высшая степень окисления кремния.
Минимальная среди основных положительных степеней окисления фосфора равна +3, а ближайшая к нему положительная — +5. Таким образом, с кислородом из оксидов P +3 2O3 и P +5 2O5 реагирует только P2O3. При этом протекает реакция доокисления фосфора кислородом от степени окисления +3 до степени окисления +5:
P +5 2O5 + O2 ≠ — реакция невозможна в принципе, т.к. +5 – высшая степень окисления фосфора.
Минимальная среди основных положительных степеней окисления серы равна +4, а ближайшая к ней по значению положительная — +6. Таким образом, с кислородом из оксидов S +4 O2, S +6 O3 реагирует только SO2. При этом протекает реакция:
2S +6 O3 + O2 ≠ — реакция невозможна в принципе, т.к. +6 – высшая степень окисления серы.
Минимальная среди положительных степеней окисления меди равна +1, а ближайшая к ней по значению — положительная (и единственная) +2. Таким образом, с кислородом из оксидов Cu +1 2O, Cu +2 O реагирует только Cu2O. При этом протекает реакция:
2Cu +1 2O + O2 =t o => 4Cu +2 O
CuO + O2 ≠ — реакция невозможна в принципе, т.к. +2 – высшая степень окисления меди.
Минимальная среди основных положительных степеней окисления хрома равна +2, а ближайшая к ней по значению положительная равна +3. Таким образом, с кислородом из оксидов Cr +2 O, Cr +3 2O3 и Cr +6 O3 реагирует только CrO, при этом окисляясь кислородом до соседней (из возможных) положительной степени окисления, т.е. +3:
Cr +3 2O3 + O2 ≠ — реакция не протекает, несмотря на то что существует оксид хрома и в большей, чем +3, степени окисления (Cr +6 O3). Невозможность протекания данной реакции связана с тем, что требуемый для ее гипотетического осуществления нагрев сильно превышает температуру разложения оксида CrO3.
Cr +6 O3 + O2 ≠ — данная реакция не может протекать в принципе, т.к. +6 – высшая степень окисления хрома.
Минимальная среди основных положительных степеней окисления марганца равна +2, а ближайшая к ней положительная — +4. Таким образом, с кислородом из возможных оксидов Mn +2 O, Mn +4 O2, Mn +6 O3 и Mn +7 2O7 реагирует только MnO, при этом окисляясь кислородом до соседней (из возможных) положительной степени окисления, т.е. +4:
2Mn +2 O + O2 =t o => 2Mn +4 O2
Mn +4 O2 + O2 ≠ и Mn +6 O3 + O2 ≠ — реакции не протекают, несмотря на то что существует оксид марганца Mn2O7, содержащий Mn в большей, чем +4 и +6, степени окисления. Связанно это с тем, что требуемый для дальнейшего гипотетического окисления оксидов Mn +4 O2 и Mn +6 O3 нагрев существенно превышает температуру разложения получаемых оксидов MnO3 и Mn2O7.
Mn +7 2O7 + O2 ≠ — данная реакция невозможна в принципе, т.к. +7 – высшая степень окисления марганца.
Минимальная среди основных положительных степеней окисления железа равна +2, а ближайшая к ней среди возможных — +3. Несмотря на то что для железа существует степень окисления +6, кислотного оксида FeO3, впрочем, как и соответствующей ему «железной» кислоты не существует.
Таким образом, из оксидов железа с кислородом могут реагировать только те оксиды, которые содержат Fe в степени окисления +2. Это либо оксид Fe +2 O, либо смешанный оксид железа Fe +2 ,+3 3O4 (железная окалина):
смешанный оксид Fe +2,+3 3O4 может быть доокислен до Fe +3 2O3:
Fe +3 2O3 + O2≠ — протекание данной реакции невозможно в принципе, т.к. оксидов, содержащих железо в степени окисления выше, чем +3, не существует.













