какая масса молекулы азота
Молярная масса азота
Молярная масса азота.
Молярная масса азота:
Молярная масса – это характеристика вещества, отношение массы вещества к его количеству.
В Международной системе единиц (СИ) единицей измерения молярной массы является килограмм на моль (русское обозначение: кг/моль; международное: kg/mol). Исторически сложилось, что молярную массу, как правило, выражают в г/моль.
Молярная масса численно равна массе одного моля вещества, то есть массе вещества, содержащего число частиц, равное числу Авогадро (NA = 6,022 140 76⋅10 23 моль −1 ).
Молярная масса, выраженная в г/моль, численно совпадает с молекулярной массой (абсолютной молекулярной массой), выраженной в а. е. м., и относительной молекулярной массой.
В свою очередь, молекулярная масса – масса молекулы. Различают абсолютную молекулярную массу (обычно выражается в атомных единицах массы, а. е. м.) и относительную молекулярную массу – безразмерную величину, равную отношению массы молекулы к 1/12 массы атома углерода 12 C.
Молярную массу обозначают M.
Молекула азота двухатомна – N2.
Молярная масса азота (M (N)) составляет 14,00643-14,00728 г/моль.
Молярная масса молекулы азота (M (N2)) составляет 28,01286-28,01456 г/моль.
Необходимо иметь в виду, что молярные массы химических элементов и простых веществ, которые они образуют – не одно и то же. Например, молярная масса кислорода как химического элемента (атома) ≈ 16 г/моль, а вещества (O2) ≈ 32 г/моль.
Молярная масса азота
Молярная масса азота
Молярную массу обычно выражают в г/моль, реже в кг/кмоль. Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr):
где κ – коэффициент пропорциональности, одинаковый для всех веществ. Относительная молекулярная масса – величина безразмерная. Её вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
Относительная атомная масса атомарного азота равна 14,0067 а.е.м. Его относительная молекулярная масса будет равна 14,0064, а молярная масса:
M(N) = Mr (N) × 1 моль = 14,0067 г/моль.
Известно, что молекула азота двухатомна – N2, тогда, относительная атомная масса молекулы азота будет равна:
Относительная молекулярная масса молекулы азота будет равна 28,0134, а молярная масса:
M(N2) = Mr (N2) × 1 моль = 28,0134 г/моль или просто 28 г/моль.
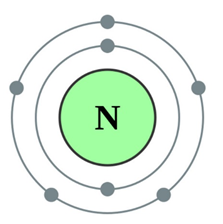
Азот представляет собой бесцветный газ, не обладающий ни запахом, ни вкусом (схема строения атома представлена на рис. 1), плохо растворимый в воде и других растворителях с очень низкими значениями температур плавления (-210 o C) и кипения (-195,8 o C).
Рис. 1. Строение атома азота.
Известно, что в природе азот может находиться в виде двух изотопов 14 N (99,635%) и 15 N (0,365%). Эти изотопы характеризуются различным содержанием нейтронов в ядре атома, а значит и молярной массой. В первом случае она будет равна 14 г/моль, а во втором – 15 г/моль.
Молекулярную массу вещества в газообразном состоянии можно определить, используя понятие о его молярном объеме. Для этого находят объем, занимаемый при нормальных условиях определенной массой данного вещества, а затем вычисляют массу 22,4 л этого вещества при тех же условиях.
Для достижения данной цели (вычисление молярной массы) возможно использование уравнения состояния идеального газа (уравнение Менделеева-Клапейрона):
где p – давление газа (Па), V – объем газа (м 3 ), m – масса вещества (г), M – молярная масса вещества (г/моль), Т – абсолютная температура (К), R – универсальная газовая постоянная равная 8,314 Дж/(моль×К).
Примеры решения задач
Определите, какой объем газа, приведенный к нормальным условиям, образуется при разложении нитрита аммония массой 16 г.
Рассчитаем количество вещества нитрита аммония (молярная масса равна – 64,06 г/моль):
Согласно уравнению реакции n(NH4NO2) :n(N2) = 1:1, т.е. n(NH4NO2) = n(N2) = 0,25 моль. Рассчитаем объем выделившегося азота:
| Задание | Вычислите объем азота (нормальные условия), который может прореагировать с магнием массой 36 г. |
| Решение | Запишем уравнение реакции химического взаимодействия магния с азотом: |
Найдем количество вещества магния, вступившего в реакцию (молярная масса равна 24 г/моль):