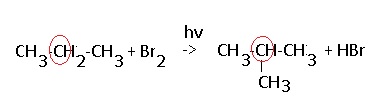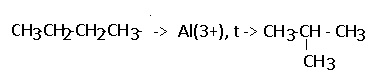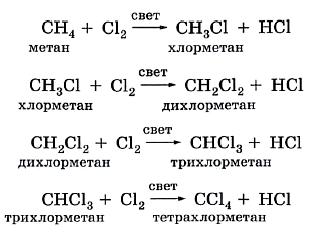какая общая формула соответствует классу алканов
Алканы
Органическая химия
По мере изучения вы поймете, что свойства вещества определяются его строением, и научитесь легко предсказывать ход реакций 😉
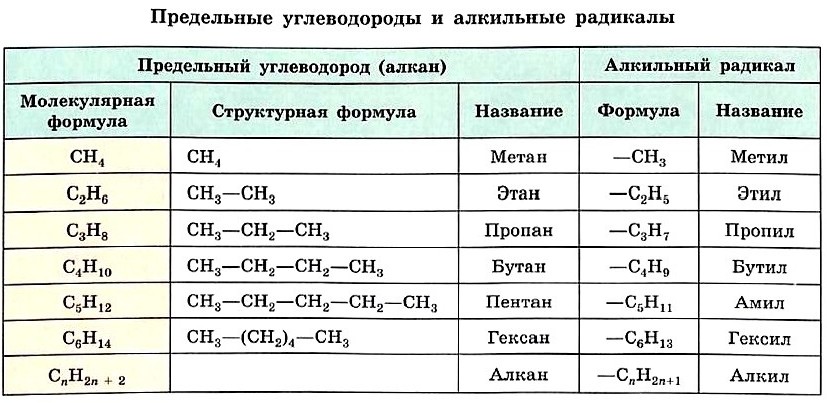
Номенклатура алканов
Гомологами называют вещества, сходные по строению и свойствам, отличающиеся на одну или более групп CH2
Названия алканов формируются по нескольким правилам. Если вы знаете их, можете пропустить этот пункт, однако я должен познакомить читателя с ними. Итак, алгоритм составления названий следующий:
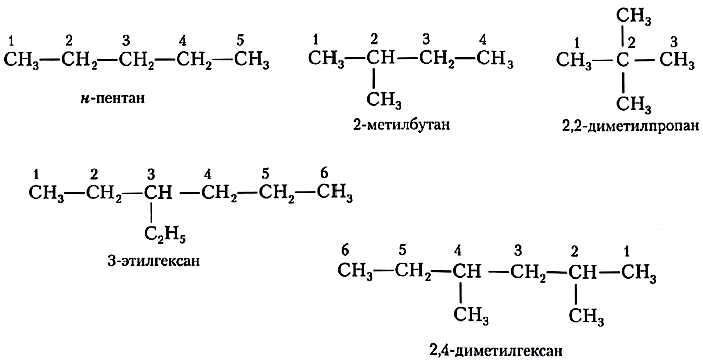
Внимательно изучите составленные для различных веществ названия ниже.
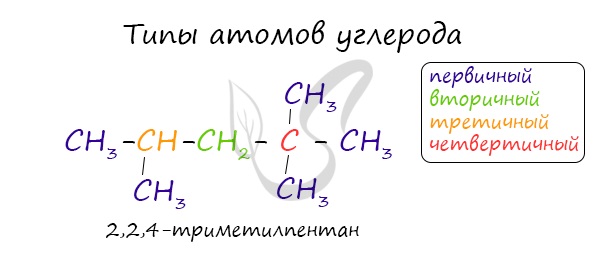
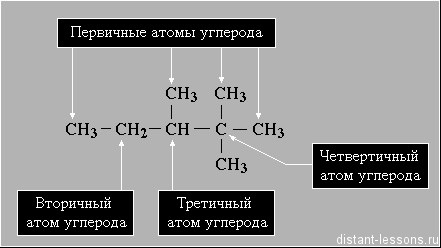
В углеводородной цепочке различают несколько типов атомов углерода, в зависимости от того, с каким числом других атомов углерода соединен данный атом. Различают первичные, вторичные, третичные и четвертичные атомы углерода.
Изомерия бывает структурной (межклассовая, углеродного скелета, положения функциональной группы или связи) и пространственной (геометрической, оптической). По мере изучения классов органических веществ вы узнаете о всех этих видах.
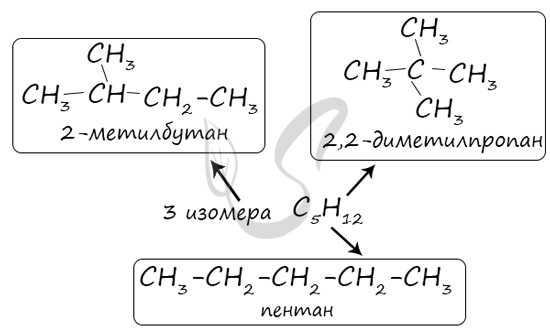
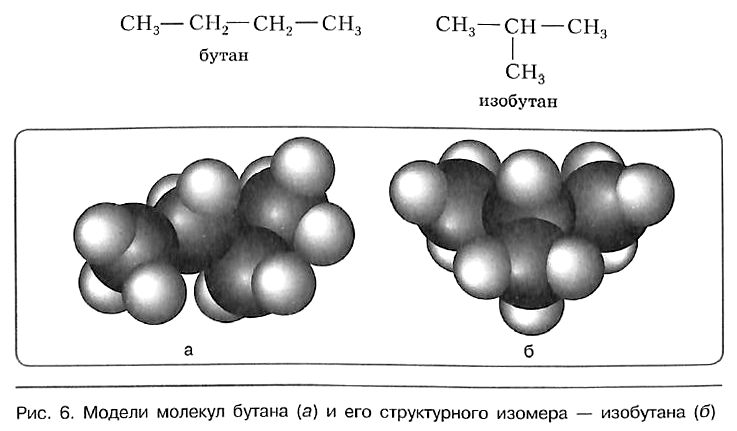
В молекулах алканов отсутствуют функциональные группы, кратные связи. Для алканов возможна изомерия только углеродного скелета. Так у пентана C5H12 существует 3 структурных изомера.
Природный газ и нефть
В состав нефти входят алканы с длинными углеродными цепочками, например: C8H18, C12H26. Путем крекинга из нефти получают алканы.
Получение алканов
В ходе крекинга нефти получается один алкан и один алкен.
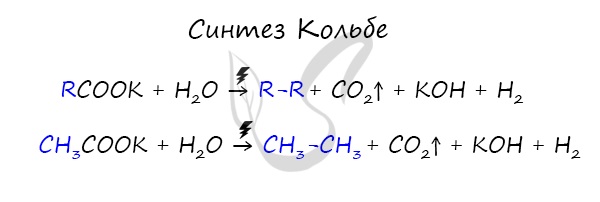
Данный синтез заключается в сплавлении соли карбоновой кислоты с щелочью, в результате образуется алкан.
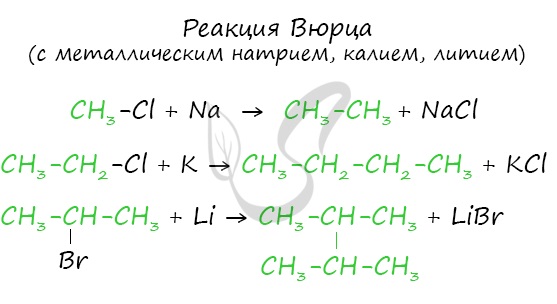
Эта реакция заключается во взаимодействии галогеналкана с металлическим натрием, калием или литием. В результате происходит удвоение углеводородного радикала, рост цепи осуществляется зеркально: в том месте, где находился атом галогена.
В ходе синтеза Гриньяра с помощью реактива Гриньяра (алкилмагнийгалогенида) получают различные органические соединения, в том числе несимметричные (в отличие от реакции Вюрца).
На схеме выше мы сначала получили реактив Гриньяра, а потом использовали его для синтеза. Однако можно записать получение реактива Гриньяра и сам синтез в одну реакцию, как показано на примерах ниже.
В результате электролиза солей карбоновых кислот может происходить образование алканов.
Химические свойства алканов
Реакции с хлором на свету происходят по свободнорадикальному механизму. На свету молекула хлора распадается на свободные радикалы, которые и осуществляют атаку на молекулу углеводорода.
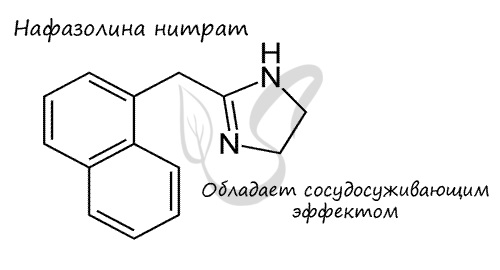
Реакция Коновалова заключается в нитровании алифатических (а также ароматических) соединений разбавленной азотной кислотой. Реакция идет при повышенном давлении, по свободнорадикальному механизму.
Все органические вещества, в их числе алканы, сгорают с образованием углекислого газа и воды.
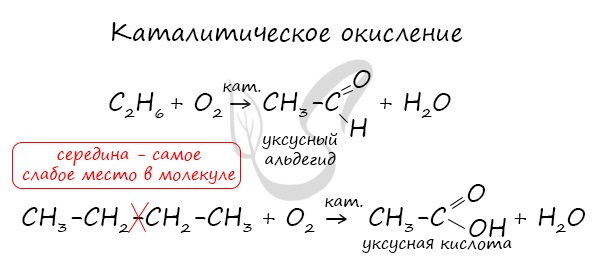
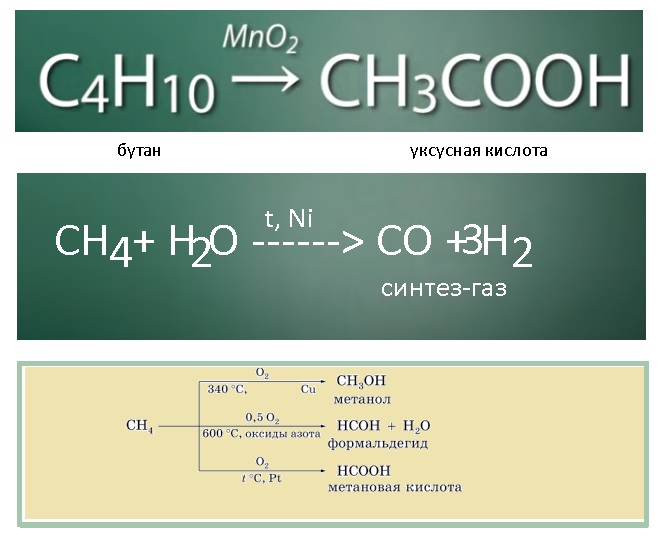
В ходе каталитического, управляемого окисления, возможна остановка на стадии спирта, альдегида, кислоты.
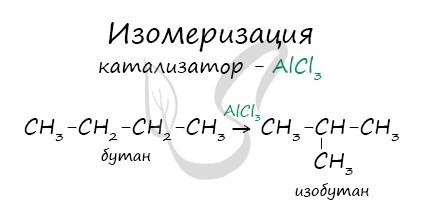
В реакциях, по итогам которых образуются изомеры, используется характерный катализатор AlCl3.
Вам уже известно, что в результате крекинга образуется один алкан и один алкен. Это не только способ получения алканов, но и их химическое свойство.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Химия, Биология, подготовка к ГИА и ЕГЭ
Предельные углеводороды —
класс алканы
(углеводороды с насыщенными связями)
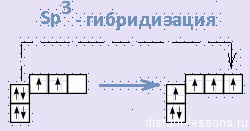
Сигма-связь (σ- )
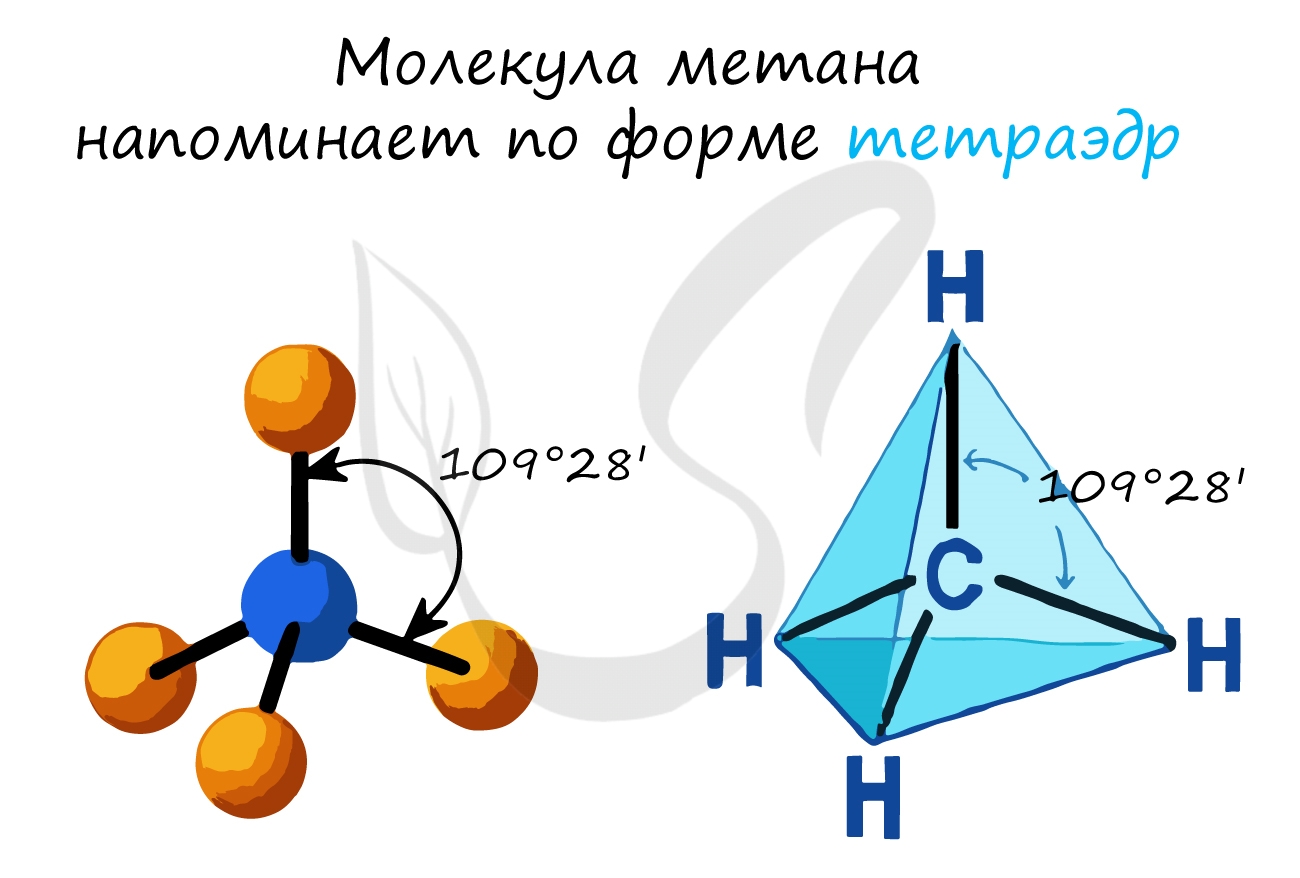
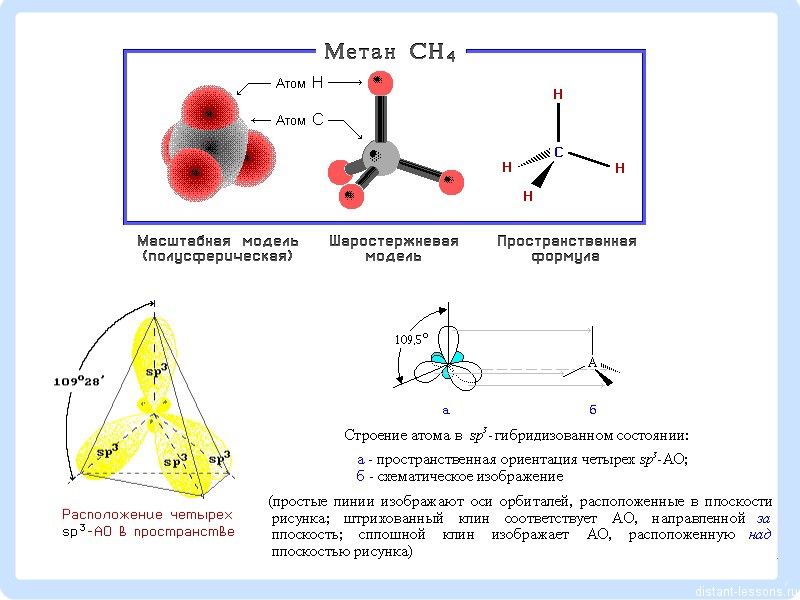
Т.е. вещества класса Алканы (парафины — старое название) – алифатические (нециклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными, насыщенными) связями в неразветвленные или разветвленные цепи. Угол между связями С-C составляет 109°28′, поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг)
Общая формула алканов:
n = числу атомов углерода.
Номенклатура веществ класса алканов строится из двух частей.
Название (приставка)
Количество атомов углерода
Формула
Физические свойства алканов:
C1-C4 — газообразные вещества;
С18-… — твердые вещества.
Алканы — довольно химически устойчивы. Между атомами насыщенная связь, поэтому вещества класса очень слабо активны.
Максимум на что они способны это:
Реакции замещения
Взаимодействие с ГАЛОГЕНАМИ:
;”>Фтор ( F2) слишком активен, он разрушает молекулы алканов, йод (I2) — наоборот, слишком малоактивен, поэтому реакции идут с хлором и бромом. Реакция идет на свету по радикальному механизму
Реакция Вюрца — «именная» реакция удлинения цепи: C 2 H 5 Cl + 2Na +Cl C 2 H 5 → C 4 H 10 + 2NaCl (из этана получили бутан)
Обратите внимание: реакция идет с бромом, но НЕ С БРОМНОЙ ВОДОЙ!
Так же как и в случае бромирования, если есть вторичный или третичный атом С, то нитрование будет идти по нему.
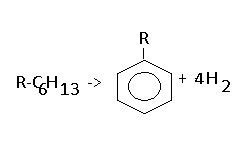
Реакции отщепления:
Реакции разложения:
Окисление алканов (горение)
как и все органические вещества, алканы горят до образования углекислого газа и воды:
Изомеризация:
Окисление алканов:
(горение тоже сюда входит, но окисление-не горение мы рассмотрим отдельно)
НЕ ОКИСЛЯЮТСЯ KMnO 4
Получение веществ класса алканы:
Вопрос из олимпиадных заданий (2015 г)
Давайте сначала определимся с атомами углерода — какие из них будут третичными
«Третичный» — атом углерода, связанный с тремя другими атомами С
название по номенклатуре ИЮПАК — 2,2-диметилбутан
В этом веществе будут 3 первичных атома (CH3-), один вторичный (-CH2-) и один четвертичный (С)
Обсуждение: “Класс алканы”
P.S. Шикарный сайт, мне он очень помогает в подготовке к экзамену!
Да, вы верно ответили. Это в ответах на тест ошибочка вкралась. Спасибо, что обратили внимание. Уже исправили! 🙂
Большое спасибо за теплый отзыв!
Здравствуйте, вы можете подсказать мне сколкьо в алканов сигма с-с с-H связей?
Добрый день!
Не совсем поняла ваш вопрос — в каком алкане?
Проще отвечу — все одинарные связи — сигма
Реакция солей карбонових кислот со щелочАМи. А если на натриевую соль по действовать гидроксидом калия? Реакция будет? Спасибо
Добрый день, Елена!
Нет, реакция идти не будет — должен образоваться карбонат одного элемента — либо натрия, либо калия, т.е. нужно на соль действовать соответствующим основанием
Реакция солей карбонових кислот со щелочАМи. А если на натриевую соль по действовать гидроксидом калия? Реакция будет? Спасибо
А каким образом собирают полученный газообразный алкаН?
Обычно это колба с газоотводной трубкой
Здравствуйте! В тесте написано, что реакция Вюрца-качественная для алканов. Разве это не способ получения? Ведь реагируют 2ГАЛОГЕНалкан+Na. Пожалуйста, объясните))) заранее спасибо
В тесте правильный ответ на этот вопрос — нет качественной реакции
здравствуйте.
вот такие две задачки.
1) напишите уравнение реакции нитрования по М.И.Коновалову изопентана. Укажите условия проведения нитрования и назовите полученные продукты. Будут ли образовываться изомеры?
2) какие вещества получатся при действии металлического натрия на следующую смесь: бромистый этил и хлористый пропил?
еще вопросы
1) какие условия проведения нитрования, может какой-то определённый интервал температуры или что-то еще?
2) будет ли продолжать замещаться водород, во вторичных углеродах и дальше?
3) будут ли образовываться изомеры? где-то находил, что будут полинитросоединения.
4) и во втором задании был БРОМИСТЫЙ этил и ХЛОРИСТЫЙ пропил, измениться ли что-то?
1)какие будут образовываться изомеры?
2)и как будет выглядеть реакция во втором задании, если взять бромистый этил и хлористый пропил, как смесь?
а почему в 1 реакции, NO2 присоединяется не к третичному атому углерода?
А куда там ему присоединиться? Все связи метилами заняты, водородов нет
Похожие задания, не могли бы вы помочь? Заранее спасибо
1) напишите уравнение реакции нитрования по
М.И.Коновалову неопентана. Укажите условия проведения нитрования и назовите полученные продукты. Будут ли образовываться изомеры?
2) какие вещества получатся при действии металлического натрия на следующую смесь: бромистый этил и бромистый изоамил?
Какая общая формула соответствует классу алканов
– это насыщенные (предельные) углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных между собой только σ-связями (одинарными связями).
Гомологический ряд алканов