какая реакция наиболее характерна для катиона кальция
Частные реакции катионов третьей аналитической группы



Реакции катиона бария Ba 2+
1. Реакция окрашивания пламени
Летучие соли бария окрашивают пламя спиртовки или горелки в желто-зеленый цвет. Реакция является фармакопейной.
Раствор соли бария (лучше BaCl2) смачивают хлороводородной кислотой и вносят в основание пламени на тонкой платиновой или нихромовой проволочке, а затем переводят в зону пламени с наивысшей температурой.
2. Разбавленная серная кислота H2SO4 и растворимые сульфаты
Выделяют даже из очень разбавленных растворов осадок сульфата бария:
Осадок не растворяется в кислотах и щелочах.
К одной капле раствора соли бария добавляют 1 каплю разбавленной H2SO4 – выпадает белый осадок BaSO4.
3. Карбонат аммония (NH4)2CO3 или другой растворимый карбонат с солями
бария дает осадок карбоната бария:
Осадок растворим в разбавленных минеральных кислотах и в уксусной кислоте. Осаждение следует вести в слабощелочной среде, лучше в аммиачной, т.к. в кислотах он растворим.
В пробирку помещают 2 капли раствора BaCl2 или Ba(NO3)2, добавляют 1 каплю разбавленного аммиака и 2 капли раствора карбоната аммония.
4. Хромат калия K2CrO4 или натрия Na2CrO4 осаждает из нейтральных или уксусно-кислыхрастворов бариевой соли хромат бария желтого цвета:
Реакцию следует проводить в слабокислой среде ацетата натрия (1 капля).
К 1 капле раствора бариевой соли добавляют 1 каплю раствора хромата калия.
5. Оксалат аммония (NH4)2C2O4 образует с солями бария осадок:
К 2 каплям раствора соли бария добавляют 2 капли раствора оксалата аммония.
Реакции катиона Ca 2+
1.Реакция окрашивания пламени.
Летучие соли кальция окрашивают пламя спиртовки в кирпично-красный цвет. Реакция является фармакопейной.
Реакция выполняется так же, как описано для катиона бария.
2. Разбавленная серная кислота H2SO4 образует с ионами кальция белый осадок сульфата кальция:
Из-за высокой растворимости сульфата кальция осаждение возможно только из достаточно концентрированных растворов солей кальция. Более полное осаждение сульфата происходит при добавлении к раствору этилового спирта.
К 3 каплям соли кальция добавляют 3-4 капли разбавленной серной кислоты. К помутневшему раствору приливают 8-10 капель этилового спирта. Наблюдают выпадение осадка.
3. Оксалата аммония (NH4)2C2O4 дает на холоде в нейтральных, уксуснокислых или слабощелочных растворах белый мелко-кристаллический осадок оксалата кальция:
Это наиболее важная качественная реакция иона Cа 2+ и является фармакопейной.
К 2 каплям раствора хлорида кальция добавляют 2 капли раствора оксалата аммония.
4. Гексацианоферрат (II) калия (желтая кровяная соль) K4[Fe(CN)6] с солями кальция образуют в слабощелочной среде белый кристаллический осадок, нерастворимый в уксусной кислоте:
В пробирку помещают 2 капли раствора хлорида кальция, добавляют 1 каплю раствора хлорида аммония и 2 капли раствора аммиака до щелочной реакции и нагревают 1-2 мин. На водяной бане. К горячему раствору прибавляют 5-6 капель 0,5 М раствора желтой кровяной соли. Вновь нагревают 2-3 мин. На водяной бане. Реакция мене чувствительна, чем с оксалатом аммония.
5. Микрокристаллоскопическая реакция. Разбавленная серная кислота образует с солями кальция иглообразные кристаллы CaSO42H2O.
На предметное стекло помещают 1 каплю раствора соли кальция и рядом 1 каплю разбавленной кислоты. Соединяют стеклянной палочкой обе капли и слегка подсушивают (но не высушивают досуха!) над водяной баней до появления каемки по кромке капли. Образующиеся кристаллы рассматривают под микроскопом.
Аналитическая химия. Катионы 3 аналитической группы
Ищем педагогов в команду «Инфоурок»
Общая характеристика катионов третьей группы
Катионы третьей группы – осаждаются серной кислотой и ее солями, которые являются групповыми реагентами. При взаимодействии с сульфатом катионы дают нерастворимые в воде сульфаты бария и стронция и плохо растворимый сульфат кальция. Они образуют также нерастворимые в воде фосфаты, сульфиты, карбонаты. Нитраты, бромиды, хлориды, гидрокарбонаты хорошо растворимы в воде.
Гидроксиды кальция, бария, стронция обладают слабощелочными свойствами и в воде растворимы плохо. Катионы бесцветны, окраска их солей зависит от аниона. Соединения кальция, бария и стронция широко применяют как реактивы, минеральные краски, строительные материалы.
Значение в медицине и фармации катионов 3-ей аналитической группы
В медицинской и фармацевтической практике применяют соли кальция и бария. Сульфат кальция или гипс применяют для наложения повязок, при изготовлении зубных порошков. Хлорид кальция, глюконат кальция, лактат кальция используют при аллергических заболеваниях, как кровоостанавливающее средство, при пониженной свертываемости крови. Карбонат кальция или мел способен снижать повышенную кислотность желудочного сока. Он входит в состав зубных порошков и паст. Соединения кальция играют важную роль в организме, входя в состав костей, тканей, крови. Они регулируют деятельность системы свертывания крови, нервные и имунные процессы, работу сердца.
Из солей бария в медицине применяется сульфат бария как рентгеноконтрасное средство при рентгеноскопии желудка и кишечника.
Действие группового реактива
Для открытия катионов 3-ей группы применяется групповой реактив – разбавленная серная кислота и ее соли. При взаимодействии катионов 3-ей группы с сульфат-ионом в в растворах образуются белые кристаллические осадки:
Наименьшую растворимость имеет сульфат бария. Сульфат стронция и кальция растворяются в воде лучше, особенно сульфат кальция, который выделяется в осадок из концентрированных солей кальция. Поэтому при проведении реакции осадок сульфата бария образуется практически мгновенно, сульфат стронция – после стояния, сульфат кальция – только из концентрированных растворов. Благодаря высокой растворимости в воде сульфат кальция образует насыщенный раствор, который может служить реактивом на катионы бария:
Насыщенный раствор сульфата стронция соответственно является реактивом на катионы бария:
Осадки сульфатов катионов 3-ей группы нерастворимы в кислотах и щелочах, лишь сульфат кальция растворим в растворе сульфата аммония ( NH 4 ) 2 SO 4 с образованием комплексной соли:
Эту реакцию иногда используют для отделения ионов кальция от остальных. В виду высокой растворимости сульфата кальция в воде его осаждение следует проводить из спирто-водных растворов (50º), растворимость CaSO 4 в них значительно снижается.
При отделении катионов 3-ей группы от других катионов с помощью сульфат-ионов образующиеся осадки нерастворимы в кислотах или щелочах. С целью улучшения их растворимости сульфаты переводят в карбонаты. Для перевода сульфатов бария, стронция и кальция в карбонаты осадок обрабатывают при нагревании многократно раствором Na 2 CO 3 :
При этом образуются осадки карбонатов бария, стронция и кальция, растворимые в кислотах:
Полученный раствор затем используют для качественного открытия отдельных ионов 3-ей группы.
Реакции катионов бария Ba 2+
Реакция с солями хромовой кислоты:
Образуется желтый кристаллический осадок хромата бария, растворимый в азотной и соляной кислотах:
В серной кислоте желтый осадок осадок хромата бария переходит в белый осадок сульфата бария:
В уксусной кислоте и других слабых кислотах осадок хромата бария нерастворим.
При взаимодействии солей бария с солями дихромовой кислоты также образуется осадок хромата бария:
При проведении реакции выделяется соляная кислота, которая частично растворяет осадок хромата бария, поэтому при применении дихроматов осаждение хромата бария происходит не полностью.
Для полного осаждения хромата бария с помощью дихроматов используют добавку солей уксусной кислоты. Соли уксусной кислоты взаимодействует с соляной кислотой, в итоге образуется слабая уксусная кислота, в которой осадок хромата бария не растворяется:
CH 3 COONa + HCl → CH 3 COOH + NaCl
Ионы стронция и кальция осадка с дихроматами не образуют, так как образующиеся хроматы кальция и стронция растворяются полностью в выделяющейся соляной или уксусной кислоте.
Реакция с солями щавелевой кислоты:
Образуется белый кристаллический осадок оксалата бария, растворимый в соляной и азотной кислотах, при нагревании – в концентрированной уксусной кислоте.
Реакция с карбонатами:
Образуется белый аморфный осадок, при нагревании переходящий в кристаллический, растворимый в соляной, азотной и уксусной кислотах.
Реакция с моногидрофосфатом натрия:
Образуется белый кристаллический осадок, растворимый в соляной, азотной и уксусной кислотах.
Реакция с гипсовой водой:
Образуется белый осадок сульфата бария.
Капельная реакция с родизонатом натрия:
CO – CO – CO – Na CO – CO – CO
BaCl 2 + │ ║ → │ ║ Ba ↓+ 2NaCl
CO – CO – CO – Na CO – CO – CO
При нанесении на фильтровальную бумажку капли нейтрального раствора соли бария и раствора родизоната натрия появляется красно-бурое окрашивание вследствие выделения осадка родизоната бария. При добавлении капли соляной кислоты красно-бурое окрашивание переходит в красное, так как родизонат бария переходит в гидрородизонат бария красного цвета.
2 │ ║ Ba+2HCl → │ ║ Ba ↓+ BaCl 2
CO – CO – CO CO – CO – COH 2
Реакция окрашивания пламени. При внесении в пламя газовой горелки летучих солей бария(хлорид, нитрат) – пламя окрашивается в желто-зеленый цвет.
Реакции катионов стронция Sr 2+
Дает осадки, аналогичные по свойствам катиону бария с солями щавелевой, угольной и хромовой кислот, с гидрофосфатами, щелочами, гипсовой водой. Но не дает осадка с дихроматами.
Капельная реакция с родизонатом натрия:
CO – CO – CO – Na CO – CO – CO
SrCl 2 + │ ║ → │ ║ Sr ↓+ 2NaCl
CO – CO – CO – Na CO – CO – CO
Реакция окрашивания пламени. При внесении летучих солей стронция (хлорид, нитрат) в пламя газовой горелки пламя окрашивается в карминово-красный цвет.
Реакции катионов кальция С a 2+
Реакция с оксалатами:
Образуется кристаллический белый осадок оксалата кальция, который растворим в минеральных кислотах и нерастворим в уксусной кислоте( в отличие от оксалатов бария и стронция).
Реакция с гексациано(2) ферратом калия K 4 [ Fe ( CN ) 6 ]:
CaCl 2 + K 4 [ Fe ( CN ) 6 ]+2 NH 4 OH → Ca ( NH 4 ) 2 [ Fe ( CN ) 6 ]↓+ 2 KCl +2 KOH
Реакция окрашивания пламени. Пламя газовой горелки при внесении солей кальция окрашивается в кирпично-красный цвет.
Анализ смеси катионов третьей аналитической группы
Т.к. осадки сульфатов катионов3-ей группы практически нерастворимы в кислотах и щелочах, проводят реакцию их перевода в карбонаты. Для этого добавляют большой избыток карбоната натрия и кипятят. При этом сульфаты переходят в карбонаты. Осадок карбонатов промывают холодной водой до нейтральной реакции фильтрата и растворяют в уксусной кислоте. В фильтрате открывают катионы 3-ей группы. Катион бария открывают реакцией с дихроматом калия. При обнаружении катиона бария, его удаляют из раствора, добавляя избыток дихромата калия. Отделяют осадок и в фильтрате обнаруживают катионы стронция и кальция. Их осаждают, добавляя избыток насыщенного раствора карбоната натрия и нагревают. Осадок карбонатов стронция и кальция промывают горячей водой до удаления ионов хромата и растворяют в уксусной кислоте. К части раствора удаляют гипсовую воду и кипятят. При наличии в растворе катиона стронция образуется осадок сульфата стронция. Его при обнаружении удаляют, осаждая раствором сульфата аммония.
После отделения стронция в фильтрате открывают кальций с помощью раствора оксалата аммония или гексациано(2) феррата калия.
Качественные реакции катионов
” data-shape=”round” data-use-links data-color-scheme=”normal” data-direction=”horizontal” data-services=”messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger”>
Важнейшие аналитические реакции катионов
При контроле качества лекарственных препаратов требуется определение подлинности содержания в них компонентов, в том числе и катионов металлов, т.е. их идентификация. Почти для каждого катиона известно значительное число разнообразных аналитических реакций. Ниже охарактеризованы только те аналитические реакции, которые чаще применяются в анализе лекарственных средств.
1. Аналитические реакции катионов первой аналитической группы: Li + , Na + , K + , NH4 +
Аналитические реакции катиона лития Li
1.1. Реакция с гидрофосфатом натрия Na2HPO4
Гидрофосфат натрия в нейтральной или слабощелочной среде образует с катионом лития белый осадок ортофосфата лития:
3Li + + НРO4 2- = Li3PO4↓+ Н +
Реакцию проводят обычно в аммиачной среде для связывания выделяющихся ионов водорода. Для увеличения полноты осаждения при проведении реакции добавляют этанол (при этом растворимость фосфата лития уменьшается). Осадок Li3PO4 растворим в кислотах и растворах солей аммония.
Предел обнаружения катионов лития данной реакции составляет 5 мкг. Мешают все катионы, образующие нерастворимые фосфаты.
Методика. В пробирку вносят 10 капель раствора солей лития, добавляют столько же капель концентрированного раствора аммиака, несколько капель этанола и 15 капель раствора гидрофосфата натрия. Через 5 минут выпадает белый мелкокристаллический осадок, растворимый в уксусной кислоте. Прибавление большого количества этанола следует избегать во избежание выделения осадка Na2HPO4.
Методика. В пробирку вносят 3-4 капли раствора солей лития, 1-2 капли концентрированного раствора аммиака и 4-5 капель раствора фторида аммония NH4F. Смесь нагревают. Медленно выпадает аморфный осадок фторида лития (осадок растворяется в уксусной кислоте).
Аналитические реакции катиона Na +
Методика. На предметное стекло наносят каплю концентрированного раствора NaCl и одну каплю концентрированного раствора К[Sb (OH)6].
Через 3-5 минут наблюдают под микроскопом образование кристаллов.
Аналитические реакции катионов калия К +
Методика. В пробирку вносят 2 капли концентрированного раствора соли калия и 2 капли свежеприготовленного концентрированного раствора Na3[Co(NO2)6]. Выпадает желтый осадок NaK2[Co(NO2)6]. Если осадок не образуется, потирают стенки пробирки стеклянной палочкой.
Методика. В пробирку вносят 2-3 капли раствора соли калия, 2-3 капли раствора гидротартрата натрия и потирают стенки пробирки стеклянной палочкой. Через некоторое время выделяется белый кристаллический осадок.
Аналитические реакции катионов аммония NH4 +
Методика. В пробирку вносят 8-10 капель раствора соли аммония, прибавляют такой же объем раствора NaOH и осторожно нагревают раствор, не допуская его кипения и разбрызгивания. Над раствором помещают влажную красную лакмусовую бумажку, не касаясь ею стенок пробирки во избежание попадания на бумажку капелек щелочного раствора. Выделяющиеся пары аммиака окрашивают бумагу в малиновый цвет.
Методика. К 1-2 каплям раствора соли аммония прибавляют 2 капли раствора реактива Несслера. Выпадает аморфный красно-бурый осадок.
В таблице 1 охарактеризованы продукты нескольких аналитических реакций катионов первой аналитической группы по кислотно-основной классификации.
2. Аналитические реакции катионов второй аналитической группы: Ag + , Hg 2+ , Pb 2+ .
Аналитические реакции катиона серебра Ag + .
Методика. В одну пробирку вносят 2-3 капли раствора NaCl, в другую – столько же капель раствора NaBr, а в третью – столько же раствора К1. В каждую пробирку добавляют по 3-5 капель раствора нитрата серебра AgNО3 и наблюдают помутнение растворов и выпадение осадков AgCl, AgBr и Agl. Испытывают растворимость осадков, добавляя в каждую пробирку по 5-10 капель концентрированного аммиака. При этом осадок AgCl растворяется полностью, AgBr – частично, Agl – не растворяется.
Аналитические реакции катиона ртути (I) Hg2 2+
2.2. Реакция с хлорид-ионами.
Катионы Hg2 2+ при взаимодействии с хлорид-ионами Сl – в растворе образуют белый осадок каломели Hg2Cl2:
Hg2 2+ +2 Сl – → Hg2Cl2↓
Осадок на свету постепенно чернеет с выделением тонкодисперсной Hg:
Hg2Cl2 → HgCl2 + Hg
Осадок не растворяется в разбавленной, но растворяется в концентрированной азотной кислоте:
Hg2Cl2 + 8HNO3 →3HgCl2 + 3Hg(NO3)2 + 2NO + 4H2O
При прибавлении к осадку каломели раствора аммиака он темнеет вследствие выделения тонкодисперсной металлической ртути:
Hg2CI2 + 2NH3 → NH2 HgCl + Hg + NH4 Cl
Реакции образования каломели и ее взаимодействие с аммиаком используются при дробном открытии ртути (I).
Методика. В пробирку вносят 4-5 капель раствора нитрата ртути (I) и прибавляют такое же количество раствора хлорида натрия. Выпадает белый осадок каломели. К осадку прибавляют несколько капель раствора аммиака – осадок чернеет.
Аналитические реакции катиона свинца Рb 2+ .
2.3. Реакция с хлорид-ионами (Сl – )
В кислых растворах (при рН 2+ + 2Сl – → РbСl2 ↓
Осадок хлорида свинца растворяется в горячей воде, но при охлаждении раствора из него снова выпадает хлорид свинца, но уже в форме игл. В разбавленных щелочных растворов вместо осадка РЬС12 выпадает осадок гидроксида свинца (II).
Методика. В пробирку вносят 3-4 капли раствора нитрата свинца Pb(NO3)2 и прибавляют 3-4 капли раствора хлорида натрия. Выпадает белый осадок РЬС12. К полученной смеси приливают – 1,5 мл дистиллированной воды и нагревают до растворения осадка. При охлаждении раствора из него снопа выпадает осадок PbС12 в виде игл.
Методика. В пробирку вносят 2-3 капли раствора Pb(NО3)2, 2-3 капли раствора ацетата натрия и 3 капли раствора хромата К2СгО4 или дихромата К2Сг2О7 калия. Выпадает желтый кристаллический осадок.
Методика. В пробирку вносят 5 капель раствора РЬ(NО3)2 и прибавляют столько же капель раствора сульфата натрия или калия, выпадает белый осадок сульфата свинца. К осадку добавляют раствор щелочи и осадок растворяется.
В таблице 2 охарактеризованы продукты нескольких аналитических реакций катионов второй аналитической группы по кислотно-основной классификации.
3.1. Реакции с сульфат-ионами (SO4 2- ).
Катионы кальция образуют с сульфат-ионами белый осадок, который при медленной кристаллизации выделяется в форме игольчатых кристаллов гипса – дигидрата сульфата кальция:
Са 2+ + SO4 2- + 2H2O → CaSO4*2H2O
Для увеличения полноты осаждения к раствору добавляют равный объем этанола.
Осадок сульфата кальция нерастворим в кислотах и щелочах, но растворяется в насыщенном водном растворе сульфата аммония с образованием комплекса:
CaSO4 + (NH 4)2SO4 → (NH4)2[Ca(SO4)2], что позволяет отделить катионы Са 2+ от катионов Sr 2+ и Ва 2+
Методика. Каплю раствора хлорида кальция СаС12 наносят на предметное стекло, прибавляют каплю раствора серной кислоты и слегка упаривают смесь. Под микроскопом наблюдают образовавшиеся игольчатые кристаллы гипса CaSО4*2H2О в виде красивых сросшихся пучков или звездочек.
3.2. Реакция с оксалатом аммония (NH4)2C2О4.
Катионы кальция образуют с оксалатом аммония белый кристаллический осадок оксалата кальция:
Ca 2+ +C2О4 2- → CaC2О4↓
Реакцию проводят в слабокислой среде (рН = 6-6,5) в присутствии уксусной кислоты, в которой оксалат кальция не растворяется.
Осадок СаС2О4 нерастворим в растворе аммиака, но растворяется в разбавленных минеральных кислотах с образованием щавелевой кислоты, например:
СаС2О4↓ + 2HCI → СаС12 + Н2С2О4
Открываемый минимум – около 100 мкг. Мешают катионы стронция, бария и другие, дающие такие же осадки.
Методика. В пробирку вносят три капли раствора СаСl2, прибавляют каплю раствора уксусной кислоты и 3 капли раствора оксалата аммония. Выпадает белый кристаллический осадок оксалата кальция.
Аналитические реакции катиона стронция Sr 2+ .
При нагревании осадка SrSО4 с раствором соды он, как и сульфат кальция, переходит в осадок SrCO3, растворимый в кислотах:
SrSО4↓ + Na2CО3 →SrCО3+ Na2SО4
SrCО3↓ + 2 HCl → SrCl2 + CО2 + H2О.
Методика. а) Реакция с “гипсовой водой”. В пробирку вносят 4 капли раствора хлорида стронция SrCl2, прибавляют 5-6 капель “гипсовой воды'”, нагревают на водяной бане и оставляют на 10-15 минут. Постепенно выделяется белый осадок сульфата стронция.
б) Реакция с серной кислотой. В пробирку вносят 1-2 капли раствора SrCl2, прибавляют 2-3 капли раствора серной кислоты. Выпадает белый кристаллический осадок сульфата стронция.
Осадок нерастворим в щелочах и кислотах. При нагревании с растворами карбонатов (например, соды) сульфат бария превращается в малорастворимый карбонат бария, который растворяется в кислотах:
BaSО4↓ + Na2CО3 → ВаСО3 ↓+ Na2SО4
BaCО3↓ + 2НС1 → BaС12 + CО2+ H2О.
Методика. В пробирку вносят 2-3 капли раствора ВаСЬ и прибавляют по каплям раствор H2SО4. Выпадает белый мелкокристаллический осадок сульфата бария.
Методика. В пробирку вносят 5 капель раствора ВаСl2 и прибавляют 5 капель раствора дихромата калия К2Сг2O7 и 4-5 капель раствора ацетата натрия CH3COONa. Выпадает желтый кристаллический осадок хромата бария.
В таблице 3 охарактеризованы продукты некоторых аналитических реакций катионов третьей аналитической группы по кислотно-основной классификации.
4. Аналитические реакции катионов четвертой аналитической группы: Zn 2+ , Al 3+ , Sn 2+ , Cr 3+ .
Аналитические реакции катиона цинка Zn 2+ .
4.1. Реакция с щелочами (NaOH, КОН и. др.).
Катионы цинка Zn 2+ образуют с гидроксидами щелочных металлов белый осадок, растворяющийся в избытке щелочи с образованием бесцветного гидрокомплекса:
Zn 2+ + 2OH – → Zn(OH)2↓
Zn(OH)2↓+ 2OH – → [Zn(OH)4] 2-
Методика. В пробирку вносят 5-6 капель раствора хлорида цинка, прибавляют 1-2 капли раствора NaOH. Выпадает белый осадок гидроксида цинка. Продолжают прибавлять по каплям раствор NaOH при перемешивании. Осадок растворяется.
В нейтральной, слабокислой или слабощелочной среде (4 2+ + S 2- → ZnS↓
Осадок не растворяется в уксусной кислоте, но растворяется в растворах минеральных кислот. Реакцию часто проводят в уксуснокислой среде, так как в этих условиях открытию Zn 2+ не мешают остальные катионы четвертой аналитической группы, за исключением олова (II).
Методика. К 2-3 каплям раствора ZnCl2 прибавляют 1-2 капли свежего раствора сульфида аммония (NH4)2S. Выпадает белый осадок сульфида цинка.
4.3. Реакция с дитизоном (дифенгштиокарбазоном).
При смешении хлороформного раствора дитизона (экстракционный реагент) с водным щелочным раствором, содержащим катионы Zn2+, образуется дитизонатный комплекс цинка красного цвета, экстрагирующийся из водной фазы в органическую. Хлороформный слой принимает более интенсивную красную окраску, чем водный. Протекание реакции предположительно можно описать следующей схемой:
Zn 2+ + H2D → [Zn(HD)2] + 2Н +
Методика. В пробирку вносят 5-10 капель раствора ZnCl2, прибавляют постепенно несколько капель раствора NaOH до растворения выпавшего осадка и около 5 капель хлороформного раствора дитизона. Пробирку встряхивают несколько раз. Хлороформный слой окрашивается в красный цвет.
Аналитические реакции катиона алюминия AI 3+ .
4.4. Реакция с щелочами.
Катионы AI 3+ при реакции с щелочами в растворах дают белый осадок гидроксида алюминия А1(ОН) 3, который растворяется в избытке щелочи с образованием гидрокомплекса [Аl(ОН) 4] – :
Аl 3+ + 3ОН – → Аl(ОН)3↓
Аl(ОН)3↓ + ОН – → [Аl(ОН) 4] –
Наиболее полное осаждение происходит при рН = 5-6. Осадок Аl(ОН) 3 растворяется в кислотах, но не растворяется в аммиаке.
При нагревании щелочного раствора комплексной соли с хлоридом аммония гидроксокомплексы алюминия разрушаются и снова выпадает осадок гидроксида алюминия:
[Аl(ОН) 4] – + NH4 + → Аl(ОН)3↓ + NH3 ↑ + Н2O
Методика. В пробирку вносят 3-5 капель раствора соли алюминия, по каплям добавляют раствор NaOH. Выпадает белый осадок. Продолжают прибавление NaOH, осадок растворяется. При добавлении к полученному раствору несколько кристаллов NH4C1 и нагревании осадок А1(ОH)3 выпадает вновь.
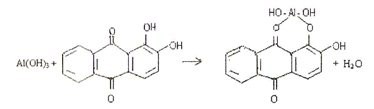
4.5. Реакция с ализарином (1,2-диоксиантрахинон).
Ализарин в реакциях с катионами алюминия Аl 3+ в аммиачной среде образует малорастворимые комплексные соединения ярко-красного цвета, называемые “алюминиевыми лаками”:
Методика. В пробирку вносят 2-3 капли раствора соли алюминия, 2-3 капли раствора щелочи (появляется белый осадок). Добавляют 1-2 капли раствора ализарина и 1-2 капли уксусной кислоты. Раствор окрашивается в красный цвет, возможно помутнение раствора.
Методика. В пробирку вносят 3-4 капли раствора соли алюминия, 2-3 капли раствора уксусной кислоты и 3-5 капель 0,01%-го раствора алюминона. Смесь нагревают на водяной бане, прибавляют несколько капель раствора аммиака до щелочной реакции (по лакмусовой бумаге) и 2-3 капли раствора карбоната аммония. Выпадает красный хлопьевидный осадок.
Аналитические реакции катиона олова (II) Sn 2+ .
4.7. Реакция с щелочами.
Соединения олова (II) при взаимодействии с щелочами выделяют из раствора белый осадок гидроксида олова Sn(OH) 2, растворимый в избытке реагента с образованием гидроксокомплекса [Sn(OH)4] 2- :
Sn 2+ + 2OН – →Sn(OH)2 ↓
Sn(OH)2↓ + 2OH – → [Sn(OH)4] 2-
Осадок Sn(OH)2 растворяется в кислотах.
Методика. В пробирку вносят несколько капель раствора соли олова (II), прибавляют по каплям раствор NaOH: вначале до выпадения белого осадка Sn(OH)2, а затем – до его растворения.
4.8. Реакция с солями висмута (III).
Олово (II) – хороший восстановитель. Так, при взаимодействии с висмутом (III) в сильно-щелочной среде оно восстанавливает висмут до металла, окисляясь до олова (IV):
2Bi 3+ + 3[Sn(OH)4] 2- + 6ОН – → 2 Bi ↓ + 3[Sn(OH)6] 2-
Металлический висмут, выделяясь в тонкодисперсном состоянии, образует осадок черного цвета.
Методика. В пробирку вносят 3-5 капель раствора олова (II) и прибавляют по каплям раствор NaOH. Вначале выпадает белый осадок гидроксида олова, который при дальнейшем прибавлении NaOH растворяется. К полученному щелочному раствору прибавляют 1-2 капли раствора нитрата висмута (III). При перемешивании смеси выпадает черный осадок металлического висмута.
Если осадок не образовался, скорее всего, неправильно создана среда (проверьте характер среды по индикаторной бумаге) или же приготовьте свежий раствор олова.
4.9. Реакции со щелочами и аммиком.
Катионы Сг 3+ с растворами щелочей или аммиака образуют осадок гидроксида хрома (III) серо-зеленого или сине-фиолетового цвета:
Сr 3+ + 3ОН – → Сr(ОН) 3 ↓
Сr 3+ + 3NH3*H2O → Сr(ОН) 3 ↓+ 3NH4 +
Осадок Сг(ОН) 3 обладает амфотерными свойствами, т.е. растворяется как в щелочах, так и в кислотах:
Сr (ОН) 3 ↓+ 3ОН – → [Cr(OH)6] 3-
Сr (ОН) 3 ↓+ 3HCl + 3H2O → [Сг(Н2O)6] 3- + 3Сl –
В растворе аммиака гидроксид хрома (III) растворяется лишь частично с образованием фиолетового комплекса [Сr(NН3) 6] 3+
Сr (ОН) 3 ↓+ 6NH3*H2O → [Сr (NН3)6] 3+ + 3ОН – + 6Н2O
Методика. В две пробирки вносят по несколько капель соли хрома (III). В них добавляют по каплям: в первую – раствор NaOH, во вторую – раствор аммиака до выпадения серо-зеленого (или сине-фиолетового) осадка. При прибавлении в первую пробирку (по каплям) раствора NaOH и перемешивании осадок растворяется с образованием раствора зеленого цвета. Добавление (по каплям) во вторую пробирку раствора аммиака приводит лишь к частичному растворению осадка. Раствор над осадком становится фиолетовым.
4.10. Реакции окисления катионов хрома пероксидом водорода и другими окислителями
Катионы Сг 3+ при взаимодействии с окислителями (пероксидом водорода, перманганатом калия и др.) окисляются до хромат-ионов СrO4 2- (желтая окраска) или до дихромат-ионов СrO7 2- (желто-оранжевая окраска):
а) Окисление пероксидом водорода.
Окисление пероксидом водорода Н2O2 проводят обычно в щелочной среде при нагревании:
2[Cr(OH)6] 3- + 3Н2O2 = 2СгO4 2- + 2OН – + 8Н2O
Методика. В пробирку вносят 2-3 капли раствора соли хрома (III), добавляют 4-5 капель 2 моль/л раствора NaOH, 2-3 капли 3%-го раствора Н2O2 и нагревают до изменения зеленой окраски раствора (цвет аквакомплексов [Сr(Н2O)6] 3- ) на желтую (цвет хромат-ионов).
б) Окисление перманганатом калия.
Перманганат калия КМnO4 в сернокислой среде при нагревании окисляет катион Cr 3+ до дихромат-иона Сr2O7 2- : 10Cr 3+ + 6МnO4 – + 11Н2O = 5Сr2O7 2- + 6Мn 2+ + 22Н +
Методика. В пробирку вносят 3-4 капли раствора соли хрома (III) (не хлорида!), прибавляют 3-4 капли раствора серной кислоты, нагревают и прибавляют к ней по каплям раствор КМnO4 до желто-оранжевой окраски раствора. При дальнейшем прибавлении реагента выпадает бурый осадок МnO2.
В таблице 4 приведены продукты некоторых аналитических реакций катионов четвертой аналитической группы по кислотно-основной классификации.
5. Аналитические реакции катионов пятой аналитической группы: Mg 2+ , Mn 2+ , Bi 3+ , Fe 2+ , Fe 3+ .
Аналитические реакции катиона магния Mg 2+ .
5.1. Реакции с щелочами и аммиаком.
Катионы Mg 2+ при действии щелочей и аммиака образуют белый аморфный осадок гидроксида магния Mg(OH):
Mg 2+ +2OH – → Mg(OH)2↓
Mg 2+ + 2NH3 * Н2O ↔ Mg(OH)2 + 2NH4 +
При реакции с аммиаком достигается неполное осаждение катионов Mg 2+ в виде гидроксида, т.к. гидроксид магния частично растворяется в растворах солей аммония, особенно концентрированных.
Осадок Mg(OH) 2 не растворяется в щелочах, но растворяется в кислотах:
Mg(OH)2 + 2Н + → Mg 2+ + 2Н2O
Методика. В две пробирки вносят по 5-6 капель раствора соли магния и прибавляют по каплям: в одну – раствор NaOH, а в другую раствор аммиака до выпадения белого аморфного осадка.
Методика. В пробирку вносят 2-3 капли раствора соли магния, прибавляют по 1-2 капли растворов NH4C1, аммиака и Na2HPO4. Раствор мутнеет и образуется белый осадок NH4MgPO4.
Методика. На предметное стекло наносят каплю раствора соли магния и прибавляют каплю щелочного раствора магнезона I. Образуется синий осадок. При малых концентрациях катионов магния осадок не выделяется, а раствор окрашивается в синий цвет.
Аналитические реакции висмута (III) Bi 3+ .
Разбавление водой растворов солей висмута (III) приводит к их гидролизу с выделением белого осадка оксохлорида висмута BiOCl:
BiCl3 + Н2O ↔ BiOCl ↓+ 2НС1
[BiC16] 3- + Н2O ↔ BiOCl ↓ + 2НС1 + 3С1 –
При прибавлении раствора НСl и нагревании осадок растворяется (обратная реакция).
5.5. Реакция восстановления висмута (III) до металла
В щелочной среде (рН
10) олово (II) восстанавливает висмут (III) до металлического висмута (0), выделяющегося в виде черного осадка. Олово (II) при этом окисляется до олова (IV):
2Bi(OH)3 + 3[Sn(OH)4] 2- → 2Bi↓ + 3[Sn(OH)6] 2-
При большом избытке щелочи и нагревании выпадает также черный осадок металлического олова вследствие протекания реакции диспропорционировапия:
2[Sn(OH)4] 2- → Sn + [Sn(OH)6] 2- + 2OH –
Методика. В пробирку вносят 2 капли солянокислого раствора хлорида олова (II), 8-9 капель 2 моль/л раствора NaOH до растворения первоначально выпавшего осадка Sn(OH)2 и добавляют 1-2 капли раствора соли висмута (III). Выпадает осадок черного цвета – металлический висмут. Особенности проведения этой реакции изложены выше (см. 4.8).
а) Окисление висмутатом. натрия в кислой среде протекает по схеме:
2Mn 2+ + 5NaBiO3+ 14Н + → 2MnO4 – + 3Bi 3+ + 5Na + + 7Н2O
Избыток висмутата натрия может маскировать окраску раствора. Методика. В пробирку вносят 5 капель концентрированной HNO3 и несколько крупинок висмутата натрия. Смесь перемешивают и добавляют к ней 1-2 капли раствора сульфата MnSO4 или нитрата Mn(NO3) 2 (но не хлорида МnCl2). Пробирку оставляют в штативе в вертикальном положении, через некоторое время раствор над реакционной смесью окрашивается в малиново-фиолетовый цвет.
б) Окисление персульфатом аммония.
Реакцию проводят в кислой среде в присутствии катализатора солей серебра (AgNO3) при нагревании:
2Мп 2+ + 5S2O8 2- + 8Н2O → 2МnO4 – + 10SO4 2 + + 16H +
Катализатором могут быть также соли кобальта и меди.
В горячем растворе возможно разложение перманганат-ионов, которое замедляется в присутствии ортофосфорной кислоты Н3РO4.
Методика. В пробирку внося несколько кристалликов (NH4)2S2O8 (или – 0,5 мл насыщенного раствора (NH4)2S2O8, прибавляют
2 мл раствора HNO3 (или H2SO4), 2-3 капли раствора AgNO3, 1-2 капли концентрированного раствора Н3РО4. Нагревают смесь до кипения и прибавляют каплю раствора соли марганца (II). Раствор окрашивается в малиновый цвет.
Аналитические реакции катиона железа (II) Fe 2+ .
Аквакатионы железа (II) [Fe(H2O)6] 2+ практически бесцветны, поэтому солей железа (II) обычно не окрашены.
5.7. Реакции с щелочами и аммиаком.
Катионы Fe 2+ образуют со щелочами и аммиаком зеленоватый осадок гидроксида железа (II) (в отсутствие кислорода воздуха он белый):
Fe 2+ + 2OН – →Fe(OH)2↓
Гидроксид Fe(OH)2 растворяется в кислотах, но не растворяется в щелочах. При стоянии на воздухе гидроксид железа (II) постепенно темнеет вследствие окисления железа (II) до железа (III) кислородом воздуха и образования красно-бурого гидроксида железа (III):
4Fe(OH)2 ↓ + O2 + 2Н2O → 4Fe(OH)3↓
В щелочной среде железо (II) легко окисляется пероксидом водорода, образуется красно-бурый осадок гидроксида железа(III):
2Fe 2+ + Н2O2 + 4OH – →2Fe(OH)3↓
Методика. а) В пробирку вносят 5-6 капель раствора железа (II) и по каплям добавляют раствор NaOH до прекращения выпадения осадка Fe(OH)2. Нa воздухе осадок постепенно темнеет.
б) К свежеприготовленному, как описано выше, белому осадку Fe(OH)2 прибавить по 2-3 капли растворов NaOH и H2О2. Окраска осадка изменяется до красно-бурой.
5.8. Реакция с калия гексацианоферратом (III) (красной кровяной солью или феррицианидом калия)
Катионы Fe 2+ реагируют с K3[Fe(CN)6] в кислой среде с образованием темно-синего осадка “турнбуленовой сини”. Ранее полагали, что состав этого осадка соответствует формуле Fe3[Fe(CN)6]2*xH2О с переменным числом молекул воды. Позднее было доказано, что уже при образовании этого осадка осуществляется окислительно-восстановительный процесс с переносом электронов от «внешнего» железа (II) к «внутреннему» железу (III):
Fe 2+ + [Fe +3 (CN)6] 3- → Fe 3+ + [Fe +2 (CN)6] 4-
Образующиеся катионы Fe 3+ и анионы [Fe +2 (CN)6] 4- дают темно-синий осадок конечного продукта Fe4 +3 [Fe +2 (CN)6]3*xH2O, названного “турнбуленовой синью”:
4Fe 3+ + 3[Fe(CN)6] 4 – →Fe4[Fe(CN)6]3↓
Суммарное уравнение реакции:
4Fe 2+ + 4[Fe +3 (CN)6] 3- → Fe4 +3 [Fe +2 (CN)6]3↓ + [Fe +2 (CN)6] 4-
По составу, структуре и свойствам осадок ”турнбуленовой сини идентичен осадку ”берлинской лазури”, получаемому при прибавлении K4[Fe(CN)6] к растворам солей железа (III).
Реакция очень чувствительна: предел обнаружения 0.05 мкг. Осадок “турнбуленовой сини'” не растворяется в кислотах, но разлагается в щелочной среде.
Методика. В пробирку вносят 2-3 капли раствора соли железа (II), прибавляют’ 1-2 капли раствора HCl и 2-3 капли раствора ферроцнанида калия K3[Fe(CN)6]. Раствор окрашивается в синий цвет и выделяется синий осадок ”турнбуленовой сини”.
Аналитические реакции катиона железа (III) Fe 3+ .
Аквакатионы железа (III) [Fe(H2O)6] 3+ окрашены в желтый цвет, поэтому водные растворы солей железа (III) имеют желтую или красновато-бурую окраску.
5.9. Реакция с щелочами и аммиаком.
Катионы Fe 3+ при взаимодействии со щелочами и аммиаком в водных растворах образуют красно-бурый осадок гидроксида железа (III):
Fe 3+ + 3ОН – → Fe(OH) 3↓
Осадок растворим в разбавленных кислотах. Он не растворяется в насыщенном растворе хлорида аммония (в отличие от осадка Ре(ОН)2), а также в растворах щелочей.
Методика. В пробирку вносят 3-4 капли раствора соли железа (Ш) и прибавляют 3-4 капли раствора NaOH. Выпадает красно-бурый осадок гидроксида железа (III).
5.10. Реакция с калия гексацианоферратом (III)(желтой кровяной солью гит ферроцгшнидом калия)
Катионы Fe 3+ в кислой среде (рН=2-3) реагируют с ферроцианидом калия с образованием темно-синего осадка “берлинской лазури”. Состав осадка описывают формулой Fe4[Fe(CN)6]3*xH2O с переменным количеством молекул воды. Этот осадок неустойчив в щелочной среде, но стабилен в кислом растворе, поэтому реакцию проводят в кислой среде при рН
2-3. Реакция образования чистой “‘берлинской лазури” протекает по схеме:
4Fe 3+ + 3[Fe(CN)6] 4- → Fe4[Fe(CN)6]3↓
Реакция высокочувствительна. Открываемый минимум около 0,05 мкг. Мешают, как и при получении “турнбуленевой сини” окислители и восстановители.
Как и в случае с “турнбуленовой синью”, осадок “берлинской лазури” не растворяется в кислотах и разлагается при прибавлении раствора щелочи:
Fe4[Fe(CN)6]3 ↓ + 12OH – → [Fe(CN)6] 4- + 4Fe(OH)3 ↓
Методика. В пробирку вносят 2-3 капли раствора соли железа (III), прибавляют 1-2 капли раствора НСl и 2 капли раствора K4[Fe(CN)6]. Раствор окрашивается в синий цвет, выпадает осадок “берлинской лазури”.
5.11. Реакция с тиоционат (роданид) ионами SCN –
Катионы Fe 3+ реагируют с тиоцинат-ионами SCN – (лучше в кислой среде при рН
3) с образованием тиоционатных комплексов железа (Ш) красного цвета:
[Fe (H2O)6.n] 3 + nSCN – → [Fe(SCN)n(H2O)6.n] 3-n + nH2O, n = 1,2,3,…6.
В зависимости от соотношения концентраций реагентов могутдоминировать комплексы различного состава. Все они имеют красную окраску и находятся в равновесии.
Реакция высокочувствительна: предел обнаружения катионов железа (III) составляет 0,25 мкг. Мешают многие вещества: окислители, восстановители, ртуть (II), фториды, фосфаты, иодиды, цитраты, тартраты и другие соединения. Катионы железа (II) не мешают.
Методика. В пробирку вносят 3-4 капли раствора соли железа (III) и прибавляют 3-4 капли раствора тиоционата аммония или калия. Раствор окрашивается в красный цвет.
В таблице 5 охарактеризованы продукты некоторых реакций катионов пятой аналитической группы по кислотно-основной классификации.
6. Аналитические реакции катионов шестой аналитической группы: Cu 2+ , Cd 2+ , Hg 2+ , Co 2+ , Ni 2+ .
Аналитические реакции катиона меди (II) Сu 2+ .
Аквакатионы меди (II) [Cu(H2O)4] 2+ окрашены в голубой цвет, поэтому водные растворы содей меди (II) имеют голубую окраску с разными оттенками.
6.1. Реакции с щелочами.
При прибавлении раствора щелочи к раствору соли меди (II) выпадает осадок гидроксида меди (II) Сu(ОН)2 имеющий окраску от сине-зеленой до голубой:
Cu 2+ +2OH – → Cu(OH)2 ↓
При последующем кипячении реакционной смеси осадок гидроксида меди разлагается до черного оксида меди (II):
Cu(OH)2 ↓ → CuO ↓ + Н2O
Осадок Сu(ОН)2 растворяется в кислотах, в растворе аммиака (с образованием комплекса [Cu(NH3)4] 2+ синего цвета), комплексообразующих органических кислотах (винная, лимонная):
Cu(OH)2 ↓ + 2Н + → Сu 2+ + 2Н2O
Cu(OH)2 ↓ + 4NH3*Н2O → [Cu(NH3)4] 2+ + 2OH – + 4Н2O
Cu(OH)2 ↓ + 2 Н2Tartr → [Cu(Tartr)2] 2- + 2H2O + 2Н +
Методика. В пробирку вносят 3-4 капли раствора соли меди (II) и прибавляют 1-2 капли раствора NaOH. Образуется осадок гидроксида меди голубого или сине-зеленого цвета. Смесь осторожно нагревают до кипения и кипятят до потемнения осадка вследствие образования черного оксида меди (II).
Методика. В пробирку вносят 3-5 капель раствора соли меди (II) и прибавляют по каплям разбавленный раствор аммиака при перемешивании смеси. Выпадающий вначале голубой (или голубовато-зеленый) осадок основной соли меди (II), затем осадок растворяется с образованием ярко-синего раствора. Прибавляют по каплям разбавленный раствор одной из кислот – HCl, HNO3 или H2SO4. Окраска раствора из ярко-синей переходит в голубую.
6.3. Реакция с тиосульфатом натрия (Na2S2O3).
При кипячении смеси подкисленного раствора соли меди (II) с избытком тиосульфата натрия Na2S2O3 происходит восстановление меди (II) до меди (I) Cu2S, кроме того образуется осадок серы. Выпадающий темно-бурый осадок – смесь сульфида меди (I) и серы. Реакция, по-видимому, протекает по схеме:
2Сu 2+ + 2S2O3 2- + 2Н2O → Cu2S↓+ S↓ + 4Н + + 2SO4 2-
Методика. В пробирку вносят 3-4 капли раствора соли меди (II), 2-3 капли разбавленного раствора H2SО4 и несколько кристалликов тиосульфата натрия. Выпадает темно-бурый осадок смеси сульфида меди (I) и свободной серы.
Аналитические реакции катиона кадмия Cd 2+ .
Аквакомплексы кадмия [Cd(H2O)n] 2+ в водных растворах бесцветны.
6.4. Реакции с щелочами и аммиаком.
При прибавлении раствора щелочи или аммиака к раствору соли кадмия выпадает белый осадок гидроксида кадмия:
Cd 2+ + 2OH – → Cd(OH)2 ↓
Осадок нерастворим в избытке щелочи, но растворяется в избытке аммиака с образованием бесцветного аммиачного комплекса [Cd(NH3)4] 2+ :
Cd(OH)2↓ + 4NH3*H2O → [Cd(NH3)4] 2+ + 4H2O
Осадок гидроксида кадмия растворяется в кислотах:
Cd(OH)2 ↓ + 2H3O + → [Cd(H2O) 3] 2+
Методика. В две пробирки вносят по 3-4 капли раствора соли кадмия. В одну из них прибавляют 1 – 2 капли растворов NaOH или КОН. Выпадает белый осадок гидроксида кадмия Cd(OH)2, который не растворяется в избытке щелочи. В другую пробирку прибавляют по каплям раствор аммиака. Образующийся вначале белый осадок гидроксида кадмия растворяется в избытке аммиака.
Аналитические реакции катиона ртути (II) Hg 2+ .
6.5. Реакция с иодидом калия (KI).
Методика. В пробирку вносят 2-3 капли раствора соли ртути (II) и прибавляют каплю разбавленного (5%) раствора иодида калия. Выпадает красный осадок иодида ртути (II) HgJ2. Осадок растворяется в избытке КJ.
Аналитические реакции катиона кобальта (II) Со 2+ .
Аквакатионы кобальта (II) [Со(Н2O)6] 2+ окрашены в розовый цвет, поэтому водные растворы солей кобальта (II) имеют розовую окраску.
6.6. Реакции с щелочами.
Катионы Со 2+ при реакции с щелочами образуют вначале синий осадок гидроксида кобальта (II) (например, CoOHCI). Окраска затем переходит в розовый осадок гидроксила кобальта (II) Со(ОН)2. Так, при взаимодействии хлорида кобальта (II) со щелочью реакция протекает по схеме:
СоСl2 + 2ОН – (недостаток) → СоОНСl ↓ (синий) + Сl –
СоОНСl ↓ (синий) + ОН – → Со(ОН)2 ↓ (розовый) + Сl –
Розовый гидроксид кобальта (II) Со(ОН)2 медленно буреет вследствие окисления кислородом воздуха до черно-бурого гидроксида кобальта (III):
4Со(ОН)2↓+ O2 + 4Н2O → 4Со(ОН)3↓
Методика. В пробирку вносят 3 капли раствора хлорида кобальта (II) и медленно, по каплям, при непрерывном перемешивании смеси, приливают водный раствор щелочи до образования синего осадка CoOHCl, переходящего при дальнейшем добавлении щелочи в розовый осадок Со(ОН)2, который через некоторое время чернеет за счет окисления до Со(ОН)3:
6.7. Реакции с аммиаком (NH3).
При реакции катионов Со 2+ с аммиаком вначале также как в 6.6 образуется синий осадок основной соли. Дальнейшее прибавление раствора аммиака приводит к растворению осадка с образованием гексамминкобальт (II) катионов грязно-желтого цвета:
СоСl2 + NH3*H2O → СоОНСl ↓+ NH4Cl
СоОНСl ↓+ 5NH3*H2O + NH4Cl → [Co(NH3)6]Cl2 + 6Н2O
На воздухе раствор постепенно принимает вишнево-красный цвет вследствие окисления Со (II) до Со (III) с образованием хлоропентаммин-кобальт – анионов [Со(NН3) 6Сl] 2+ вишнево-красного цвета:
4[Со +2 (NН3)6]Сl2 + O2 + 6Н2O → 4[Co +3 (NH3)5Cl](OH)2 + 4NH4Cl
В присутствии пероксида водорода и солей аммония реакция окисления [Со(NH3)6] 2+ до [Со(NН3)6С1] 2+ протекает мгновенно:
2[Co(NH3)6]Cl2 + H2O2 + 2NH4C1 + 2H2O → 2[Co(NH3)5Cl]Cl2 + 4NH3*H20
Методика. В пробирку вносят 3 капли раствора хлорида кобальта (II) и медленно, по каплям, прибавляют раствор аммиака до выпадения синего осадка CoOHCl, затем несколько кристаллов хлорида аммония и продолжают прибавление раствора аммиака при перемешивании смеси до полного растворения осадка и образования желтого раствора. При стоянии на воздухе раствор постепенно меняет окраску на вишнево-красную.
Методика. В пробирку вносят 2-3 капли раствора соли кобальта (II), прибавляют 8-10 капель насыщенного раствора тиоциоиата калия KNCS или аммония NH4NCS (или несколько кристаллов одной из этих солей). 5-6 капель органического растворителя (изоамилового спирта) и встряхивают смесь. Верхний слой органической фазы окрашивается в синий цвет.
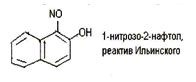
Кобальт (II) в этой реакции окисляется до кобальта (III), который с 1-нитрозо-2-нафтолом образует внутрикомплексное соединение, выделяющееся в виде пурпурно-красного осадка. Если 1-нитрозо-2-нафтол (реактив Ильинского) условно обозначить HL, реакцию можно описать схемой (после окисления кобальта):
Со 3+ + 3HL→ [CoL3] +3H +
Реакцию проводят в нейтральной или слабокислой среде. Мешают катионы меди (II).
Методика. В пробирку вносят 2-3 капли раствора соли кобальта (II), 1-2 капли уксусной кислоты, 2-3 капли 1%-го раствора реактива Ильинского. При осторожном нагревании наблюдают выделение пурпурно-красного осадка внутрикомплексного соединения.
Аналитические реакции катиона никеля (II) Ni 2+ .
Аквакатионы никеля (II) [Ni(H2O)6] 2+ окрашены в зеленый цвет, поэтому водные растворы солей никеля (II) имеют зеленую окраску.
6.10. Реакция со щелочами.
Катионы никеля (11) Ni 2+ осаждаются щелочами из водных растворов в виде малорастворимого гидроксида никеля. (II) Ni(OH)2 зеленого цвета:
Ni 2+ + 2OН – → Ni(OH)2↓
Осадок растворяется в растворах кислот и аммиака:
Ni(ОН)2 ↓ + 2Н + →Ni 2+ + 2Н2O
Ni(ОН)2 ↓ + 6NH3*H2O → [Ni(NH3)6] 2+ + 2OН – + 6Н2O
Методика. В пробирку вносят 2-3 капли раствора соли никеля (II) и прибавляют по каплям при перемешивании раствор щелочи. Выпадает светло-зеленый осадок.
Аммиак осаждает из растворов солей никеля (II) светло-зеленые осадки основных солей никеля (II), например:
Ni(NO3)2 + NH3*H2O → NiOHNO3↓+ NH4NO3
NiCl2 + NH3*H2O → NiOHCI↓ + NH4C1
2NiSO4 + NH3*H2O → (NiOH)2SO4↓+ (NH4)2SO4 и т.д.
В избытке аммиака осадок основной соли никеля (II) растворяется с образованием комплексных гексаминникель (II) – катионов синего цвета, например:
NiOHCI↓ + 6NH3*H2O → [Ni(NH3)6] 2+ + OH – + Сl – + 6H2O
Методика. В пробирку вносят 2-3 капли раствора хлорида никеля (II) NiCl2 (нитрата Ni(NO3)2 или сульфата NiSO4) и прибавляют по каплям при перемешивании раствор аммиака до выпадения зеленого осадка NiOHCl. При перемешивании продолжают добавление концентрированного раствора аммиака до полного растворения осадка и образования синего цвета.
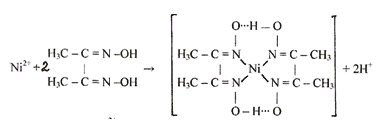
6.12. Реакция с реактивом Чугаева (диметилглиоксимом).
Катионы никеля Ni 2+ при взаимодействии с диметилглиоксимом при рН = 6-9 образуют малорастворимое в воде внутрикомплексное соединение розово-красного цвета бисдиметилглиоксиматоникель (II):
Методика. В пробирку вносят 3-4 капли раствора соли никеля (II), прибавляют 3-4 капли концентрированного аммиака и 1 каплю спиртового раствора диметилглиоксима. Выпадает розово-красный осадок комплекса.
В таблице 6 охарактеризованы продукты некоторых аналитических реакций катионов шестой аналитической группы по кислотно-основной классификации.
Таблица 2. Продукты некоторых аналитических реакций катионов второй аналитической группы по кислотно-основной классификации
Реагент
Продукты аналитических реакций