какая жидкость тяжелее воды и не смешивается
Плотность жидкостей

Множество веществ способны находится в жидком состоянии. Жидкости – вещества различного происхождения и состава, которые обладают текучестью, — они способны изменять свою форму под действием некоторых сил. Плотность жидкости – это отношение массы жидкости к объёму, который она занимает.
Рассмотрим примеры плотности некоторых жидкостей. Первое вещество, которое приходит в голову при слове «жидкость» — это вода. И это вовсе не случайно, ведь вода является самой распространённой субстанцией на планете, и поэтому её можно принять за идеал.
Плотность воды равна 1000 кг/м 3 для дистиллированной и 1030 кг/м 3 для морской воды. Поскольку данная величина тесно взаимосвязана с температурой, стоит отметить, что данное «идеальное» значение получено при +3,7°С. Плотность кипящей воды будет несколько меньше – она равна 958,4 кг/м 3 при 100°С. При нагревании жидкостей их плотность, как правило, уменьшается.
| Жидкость | Температура, °С | Плотность жидкости, кг/м 3 |
|---|---|---|
| Анилин | 0…20…40…60…80…100…140…180 | 1037…1023…1007…990…972…952…914…878 |
| Антифриз 65 (ГОСТ 159-52) | -60…-40…0…20…40…80…120 | 1143…1129…1102…1089…1076…1048…1011 |
| Ацетон C3H6O | 0…20 | 813…791 |
| Белок куриного яйца | 20 | 1042 |
| Бензин | 20 | 680-800 |
| Бензол C6H6 | 7…20…40…60 | 910…879…858…836 |
| Бром | 20 | 3120 |
| Вода | 0…4…20…60…100…150…200…250…370 | 999,9…1000…998,2…983,2…958,4…917…863…799…450,5 |
| Вода морская | 20 | 1010-1050 |
| Вода тяжелая | 10…20…50…100…150…200…250 | 1106…1105…1096…1063…1017…957…881 |
| Водка | 0…20…40…60…80 | 949…935…920…903…888 |
| Вино крепленое | 20 | 1025 |
| Вино сухое | 20 | 993 |
| Газойль | 20…60…100…160…200…260…300 | 848…826…801…761…733…688…656 |
| Глицерин C3H5(OH)3 | 20…60…100…160…200…240 | 1260…1239…1207…1143…1090…1025 |
| ГТФ (теплоноситель) | 27…127…227…327 | 980…880…800…750 |
| Даутерм | 20…50…100…150…200 | 1060…1036…995…953…912 |
| Желток яйца куры | 20 | 1029 |
| Карборан | 27 | 1000 |
| Керосин | 20 | 802-840 |
| Кислота азотная HNO3 (100%-ная) | -10…0…10…20…30…40…50 | 1567…1549…1531…1513…1495…1477…1459 |
| Кислота пальмитиновая C16H32O2 (конц.) | 62 | 853 |
| Кислота серная H2SO4 (конц.) | 20 | 1830 |
| Кислота соляная HCl (20%-ная) | 20 | 1100 |
| Кислота уксусная CH3COOH (конц.) | 20 | 1049 |
| Коньяк | 20 | 952 |
| Креозот | 15 | 1040-1100 |
| Кровь человека | 37 | 1050-1062 |
| Ксилол C8H10 | 20 | 880 |
| Купорос медный (10%) | 20 | 1107 |
| Купорос медный (20%) | 20 | 1230 |
| Ликер вишневый | 20 | 1105 |
| Мазут | 20 | 890-990 |
| Масло арахисовое | 15 | 911-926 |
| Масло машинное | 20 | 890-920 |
| Масло моторное Т | 20 | 917 |
| Масло оливковое | 15 | 914-919 |
| Масло подсолнечное (рафинир.) | -20…20…60…100…150 | 947…926…898…871…836 |
| Мед (обезвоженный) | 20 | 1621 |
| Метилацетат CH3COOCH3 | 25 | 927 |
| Молоко | 20 | 1030 |
| Молоко сгущенное с сахаром | 20 | 1290-1310 |
| Нафталин | 230…250…270…300…320 | 865…850…835…812…794 |
| Нефть | 20 | 730-940 |
| Олифа | 20 | 930-950 |
| Паста томатная | 20 | 1110 |
| Патока вареная | 20 | 1460 |
| Патока крахмальная | 20 | 1433 |
| ПАБ | 20…80…120…200…260…340…400 | 990…961…939…883…837…769…710 |
| Пиво | 20 | 1008-1030 |
| ПМС-100 | 20…60…80…100…120…160…180…200 | 967…934…917…901…884…850…834…817 |
| ПЭС-5 | 20…60…80…100…120…160…180…200 | 998…971…957…943…929…902…888…874 |
| Пюре яблочное | 0 | 1056 |
| Раствор поваренной соли в воде (10%-ный) | 20 | 1071 |
| Раствор поваренной соли в воде (20%-ный) | 20 | 1148 |
| Раствор сахара в воде (насыщенный) | 0…20…40…60…80…100 | 1314…1333…1353…1378…1405…1436 |
| Ртуть | 0…20…100…200…300…400 | 13596…13546…13350…13310…12880…12700 |
| Сероуглерод | 0 | 1293 |
| Силикон (диэтилполисилоксан) | 0…20…60…100…160…200…260…300 | 971…956…928…900…856…825…779…744 |
| Сироп яблочный | 20 | 1613 |
| Скипидар | 20 | 870 |
| Сливки молочные (жирность 30-83%) | 20 | 939-1000 |
| Смола | 80 | 1200 |
| Смола каменноугольная | 20 | 1050-1250 |
| Сок апельсиновый | 15 | 1043 |
| Сок виноградный | 20 | 1056-1361 |
| Сок грейпфрутовый | 15 | 1062 |
| Сок томатный | 20 | 1030-1141 |
| Сок яблочный | 20 | 1030-1312 |
| Спирт амиловый | 20 | 814 |
| Спирт бутиловый | 20 | 810 |
| Спирт изобутиловый | 20 | 801 |
| Спирт изопропиловый | 20 | 785 |
| Спирт метиловый | 20 | 793 |
| Спирт пропиловый | 20 | 804 |
| Спирт этиловый C2H5OH | 0…20…40…80…100…150…200 | 806…789…772…735…716…649…557 |
| Сплав натрий-калий (25%Na) | 20…100…200…300…500…700 | 872…852…828…803…753…704 |
| Сплав свинец-висмут (45%Pb) | 130…200…300…400…500..600…700 | 10570…10490…10360…10240…10120..10000…9880 |
| Стекло жидкое | 20 | 1350-1530 |
| Сыворотка молочная | 20 | 1027 |
| Тетракрезилоксисилан (CH3C6H4O)4Si | 10…20…60…100…160…200…260…300…350 | 1135…1128…1097…1064…1019…987…936…902…858 |
| Тетрахлордифенил C12H6Cl4 (арохлор) | 30…60…150…250…300 | 1440…1410…1320…1220…1170 |
| Толуол | 0…20…50…80…100…140 | 886…867…839…810…790…744 |
| Топливо дизельное | 20…40…60…80…100 | 879…865…852…838…825 |
| Топливо карбюраторное | 20 | 768 |
| Топливо моторное | 20 | 911 |
| Топливо РТ | -60…-40…0…20…40…60…100…140…160…200 | 836…821…792…778…764…749…720…692…677…648 |
| Топливо Т-1 | -60…-40…0…20…40…60…100…140…160…200 | 867…853…824…819…808…795…766…736…720…685 |
| Топливо Т-2 | -60…-40…0…20…40…60…100…140…160…200 | 824…810…781…766…752…745…709…680…665…637 |
| Топливо Т-6 | -60…-40…0…20…40…60…100…140…160…200 | 898…883…855…841…827…813…784…756…742…713 |
| Топливо Т-8 | -60…-40…0…20…40…60…100…140…160…200 | 847…833…804…789…775…761…732…703…689…660 |
| Топливо ТС-1 | -60…-40…0…20…40…60…100…140…160…200 | 837…823…794…780…765…751…722…693…879…650 |
| Углерод четыреххлористый (ЧХУ) | 20 | 1595 |
| Уроторопин C6H12N2 | 27 | 1330 |
| Фторбензол | 20 | 1024 |
| Хлорбензол | 20 | 1066 |
| Этилацетат | 20 | 901 |
| Этилбромид | 20 | 1430 |
| Этилиодид | 20 | 1933 |
| Этилхлорид | 0 | 921 |
| Эфир | 0…20 | 736…720 |
| Эфир Гарпиуса | 27 | 1100 |
Форум химиков
тяжелая жидкость. Что можно найти?
тяжелая жидкость. Что можно найти?
Сообщение Ist » Пн окт 31, 2005 11:31 am
Доброе время суток.
Помогите решить такую проблему:
нужно жидкое вещество(или смесь, раствор) обладающее следующими характеристиками
1. Имеющее как можно большую плотность (больше 2 плотности воды),равномерно распределенную по всему объему (т.е. состав кот-ой. не расслаиваится и не осаждается.)
2. хорошую текучесть (
как у воды).
3. Неагрессивное, экологичное, безопасное для здоровья чел. и о.с. при хранении в открытом объеме.
4. дешевое и легкодоступное
5. Сохраняющее выешеперечисленные характеристики длительное время при н.у.
Сообщение ИСН » Пн окт 31, 2005 12:32 pm
Сообщение AndrejЪ » Пн окт 31, 2005 12:36 pm
Сообщение eukar » Пн окт 31, 2005 12:38 pm
Сообщение AndrejЪ » Пн окт 31, 2005 12:41 pm
Сообщение eukar » Пн окт 31, 2005 12:55 pm
Сообщение AndrejЪ » Пн окт 31, 2005 1:01 pm
Re: тяжелая жидкость. Что можно найти?
Сообщение avor » Пн окт 31, 2005 1:20 pm
как у воды).
3. Неагрессивное, экологичное, безопасное для здоровья чел. и о.с. при хранении в открытом объеме.
4. дешевое и легкодоступное
5. Сохраняющее выешеперечисленные характеристики длительное время при н.у.
А вообще у вас очень много противоречивых требований.
Наиболее подходящими будет пожалуй хлороформ. Но и он на открытом воздухе не стоит и для здоровия безвреден весьма условно.
Еще возможно какая нибудь фторброморганика. Но она вам в такую копейку встанет что мало не покажется. Перфтордекалин 1 кг стоит 100уе.
Что касается глицерина, то он напрочь не подходит по причине высокой вязкости.
Сообщение Sovetnik » Пн окт 31, 2005 4:17 pm
Сообщение slavert » Пн окт 31, 2005 4:31 pm
Сообщение Iskander » Пн окт 31, 2005 9:44 pm
Сообщение Ist » Вт ноя 01, 2005 1:45 am
Вот что удалось мне найти через поиск:
жидкость Туле (3,19 г/см3) насыщенный водный раствор комплексного соединения K2Hg4
Жидкость Сушина (3,45 г/см3). насыщенный водный раствор комплекса Ba[Hg]4J
водные растворы KI, CdI2 (2.2-2.9г/см3)
бромоформ СНВг3, ( 2,9 г/см3)
жидкость Клеричи (4-4,9 г/см3) Раствор формиата и малоната таллия (небезопасна)
Йодистый метилен(дийодметан) CH2I2 (3,30-3.6г.см3). цена 1800-2000р/кг
А насколько интенсивное перемешивание необходимо? и что такое ФМЖ?
Кстати, ртуть, действительно, можно чем-нибудь залить что бы избежать вредного воздействия?
Сообщение eukar » Вт ноя 01, 2005 9:33 am
Сообщение Ist » Вт ноя 01, 2005 11:52 am
Я не знаю вязкие или нет будут растворы соли.. если да то они мне конечно не поджодят.
и изменямемость в процессе хранения тоже конечно не нужна.
Вышеперечисленные жидкости в основном по плотности подобраны, а подробной инф. что бы проверить удовлетворяют ли они вышеперечисленным требованиям, я не нашел.. собсно потому и спрашиваю здесь.
Поправка по поводу безвредности:
жидкость должна находиться в открытом объеме, но сверху ее не “трогают” т.е. в принципе, наверно можно хранить ее под верхним слем какой нить. другой жидкости (безопасной).
на дне, переодически сущ. не очень активное перемешивание.
Сообщение avor » Вт ноя 01, 2005 1:22 pm
Ртуть, кадмий и таллий жутко ядовиты особенно последний. Он еще и дорог самый безобидный и дешевый кадмий. Но утилизировать его просто сбросив в воду вам не дадут точно. Что касается органики они не дешевы особенно иодистый метилен и что характерно нестойки на свету, а иодистый метилен и на воздухе.
Так что из всегь перечисленного вам более менее, но совершенно не удовлетворяя полностью вашим условиям подойдут.
пожалуй калий иод кадмиевые соли и бромоформ.
Но они не безобидны особенно кадмий, не дешевы, и не стойки.
Что касается цен, то цена на иодистые соединения зависит от цены на иод, килограмм стоит порядка 25 уе. Бромоформ наверное дешевле, но дороже хлороформа раза в два три. причем цены зависят от поставщика и колличества в партии ну и качества бромоформа.
Сообщение Iskander » Вт ноя 01, 2005 9:39 pm
“А насколько интенсивное перемешивание необходимо? и что такое ФМЖ?
Кстати, ртуть, действительно, можно чем-нибудь залить что бы избежать вредного воздействия?”
Вообще-то интенсивное. Но оно очень сильно зависит от формы сосуда и способа перемешивания. У нас перемешивала струя жидкости с расходом порядка 10 литров в минуту при объёме ёмкости 30 литров. Механическая мешалка будет работать иначе.
Сформулируйте задачу конкретнее. Что надо сделать и сколько той жидкости потребуется.
Взболтать, но не смешивать
Все знают, что вода с маслом не смешивается.
Кто помнит школьную физику, легко назовёт третью жидкость, не смешивающуюся с этими двумя: ртуть.
Вопрос: а сколько всего известно взаимно нерастворимых жидкостей при условиях, близких к нормальным?
Тогда вопрос №2: а сколько можно найти взаимно несмешиваемых жидкостей, которые не страшно принести домой, чтобы показать демку детям?
Мне удалось собрать пять. Собственно, их сливанием вот в эту пробирку мы в статье и займёмся.
1. Рафинированное растительное масло:
В данном случае из виноградных косточек. Состоит оно главным образом из эфиров линолевой и олеиновой кислот. Слово “кислота” пусть не введёт никого в заблуждение. Обе молекулы — это главным образом длинные углеводородные “хвосты” вида *-(CH2)n-CH3. Они и отвечают за гидрофобность. По какой причине вместо масла вполне годится любой жидкий углеводород (пентан, гексан) или их смесь (бензин, керосин). Однако масло менее огнеопасно и покупается в обычном продуктовом магазине.
2. Подкрашенная голубой краской вода H2O:
3. Силиконовое масло:
Силиконовое масло — это смесь низкомолекулярных полимеров с общей формулой вида (C2H6OSi)n. Добытая на Амазоне разновидность используется как загуститель красок и оказалась вязка, как хороший мёд. Если повторять опыт, стоит поискать более текучие разновидности.
Эта жидкость “устаканилась” между водой и маслом, в соответствии с промежуточным значением своей плотности.
4. Расплавленный галлий Ga:
Галлий плавится при +29.8 C. Поэтому пробирка на время помещена в банку с тёплой водой.
Коллекционные количества галлия легко приобретаются в интернете, хотя бы на Амазоне. Металл этот достаточно безопасен, чтобы брать его в руки, и не образует ядовитых испарений. Однако, соприкасаясь с твёрдыми поверхностями и кожей, сильно пачкает их тёмным слоем оксида галлия. Этот оксид растворим в пищевых кислотах, а растворимые соли галлия могут быть и токсичными. Поэтому после работы всё, что с галлием соприкасалось, надо отмывать от его оксида. Обыкновенная тёплая мыльная вода прекрасно справляется с этой задачей.
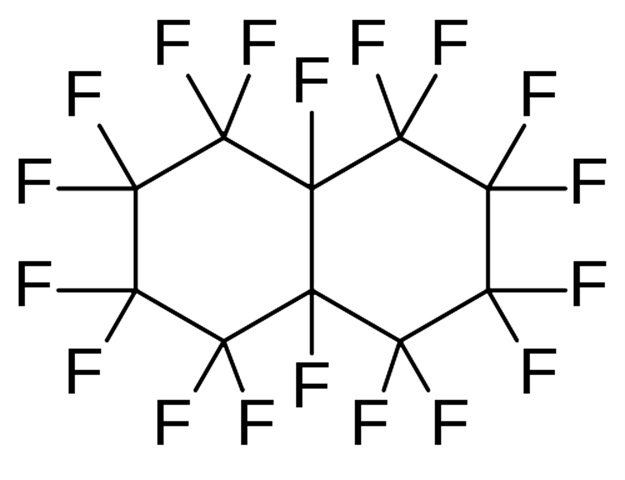
5. И последнее вещество — перфтородекалин (perfluorodecalyn) C10F18:
Эта жидкость заметно тяжелее воды, поэтому собралась над галлием. Состоит она исключительно из фтора и углерода:
В Штатах производители продают это вещество только бизнесам, имеющим легитимную потребность в работе с ним. К счастью, незначительные его количества (5-10 грамм) вполне законно приобретаются у частных лиц на eBay.
Ядовитым в строгом смысле этого слова перфтородекалин не является. Его даже добавляют в некоторые виды косметики, а близкородественные ему соединения используют в качестве основного компонента искусственной крови. Однако пары более лёгких его “родственников” вызывают отключку сознания и используются для наркоза, и мне не хотелось проверять, обладает ли конкретно эта жидкость теми же свойствами. Кроме того, в вопросе о воздействии его на глаза найденные статьи демонстрировали странное разногласие. Так что работал я с ним в очках, перчатках, на открытом воздухе, и не подпускал зрителей к пробирке слишком близко. На всякий случай.
6. Конечное состояние
Качественно перемешав все жидкости стеклянной палочкой, я дал им денёк отстояться, и получил в итоге вот такую картину:
Любопытно, что между некоторыми компонентами возникли тонкие слои дополнительных фаз, вероятно, из-за небольшой взаимной растворимости.
Написал конструктор, напиши и деструктор
Что со всей этой смесью потом делать?
Воду и масло спокойно выливаем. Силиконовое масло — в мусор. Конечные продукты его разложения — вода, углекислый газ и песок, хотя процесс этот небыстрый.
Галлий можно собрать пипеткой, слить в спичечный коробок, заморозить и держать дома для будущих опытов. Только не замораживайте его в стеклянной посуде. Этот металл здорово расширяется при застывании и рвёт её в клочья:
Если всё-таки не хочется держать галлий дома, везите его на свалку для тяжёлых металлов и/или токсичных отходов. Или подарите знакомым химикам, пусть найдут ему применение.
Сложнее всего избавиться от перфтородекалина. Вещество это химически настолько стойкое, что разрушить его в домашних условиях до безопасных компонент практически невозможно. Из-за той же стойкости разлагаться в природе оно будет тысячелетиями, путями не вполне понятными, и с неясным пока воздействием на биосферу за всё это время. Так что, по-хорошему, я бы рекомендовал связаться с организациями, перерабатывающими отходы от настоящих химических лабораторий, и сдать перфтородекалин им. Можно через знакомых химиков, что я и сделал.
Спасибо за чтение, хорошего всем дня! Кому надо, вот PDF.
Какие жидкости тяжелее воды?
Многие жидкости тяжелее воды,даже соленая вода тяжелее чистой воды.
Грязь,жидкая глина,жидкий металл,ртуть,металлы в жидком состоянии,молоко,хлороформ,этилиодид,глицерин,серная кислота- это только пример жидкостей,которые обладают большей массой чем вода,это связано с большей плотностью данных жидкостей.
Чем больше плотность в жидкости,тем больше она будет весить скажем в 1 литре.
Жидкости с плотностью выше 1 г/см 3 (такова плотность самой воды) будут тяжелее неё. К ним относятся и насыщенные растворы солей тяжелых металлов (свинца, висмута, ртути), и многие кислоты. А к самым тяжелым жидким веществам можно смело отнести формиат и маллонат таллия (в комплексе образует жидкости Клеричи с плотностью 4,32 г/см3). Данную жидкость используют для разделения минералов по плотности.
Если вода в бассейне с химикатами, а она с химикатами скорее всего, раз бассейн не детский, а достаточно большой и объемный, то такой водой поливать не желательно. Там как минимум есть хлор, и всякие противомикробные и противогрибковые средства.
Объем воды такой большой, что иногда ее просто некуда больше деть, кроме как в огород, так как чаще всего, такие бассейны, каркасные, либо надувные, по типу Интекс, устанавливают именно на дачах. Но лучше этого не делать, пустить шланг с водой, максимально мимо растений, не для полива, либо в яму, если она есть.
В самом крайнем случае, можно чуть-чуть полить цветы, но и то, не всякие такой полив перенесут.
Лучше всего выполаскивает мыло тёплая вода. Холодная может сбить мыло, горячая усиливает пенообразование и замедляет выпласкивание. Это касается как натуарльного мыла, так и синтетических моющих средств.
Стихийные духи это первичная полевая форма жизни возникшая на земле. Их задача помочь природе в создании более плотной жизни в том числе и нас с вами. Они до сих пор выполняют свою задачу, но люди от них отделились под влиянием религии, образования и всей прочей псевдодуховности. Они остались так же дружествены к человеку, но человек от них закрывается, что идёт людям во вред. Сейчас под влиянием веры их называют чертями или нечистыми, что означает не в чести или не уважаемые.
Ответ: варан.
Тяжелая вода: что это такое и где она применяется, как получить такую жидкость в домашних условиях – физические свойства воды и химическая формула
Вы наверняка о ней слышали, но уделяли ли ей достаточно внимания? Чтобы ответить, рассмотрим, что собой представляет тяжелая вода: что это такое, где применяется, чем отличается от обычной, что будет, если регулярно употреблять ее в быту и так далее.
Сразу отметим: сегодня она используется все активнее, особенно в химической промышленности и в экспериментальной медицине. Ученые подбирают различные ее дозировки для проведения глобальных исследований, призванных улучшить приплод и увеличить вес домашних животных, а также побороть раковые опухоли. Успехи переменные, но они есть (плюс многие изыскания рассчитаны на длительную перспективу, и их результаты пока не оценить), поэтому работы в этих направлениях продолжаются, чему только способствует общее развитие технологий.
Что значит термин «тяжелая вода»
Она представляет собой оксид — либо водорода 2H (вместо легкого 1H в обычных условиях), либо дейтерия D, то есть изотопа, содержащего на один нейтрон больше, чем в стандартном случае. Такая замена оборачивается повышением удельной массы на 10%.
Немного справочной информации:
В природных источниках соотношение D к H сегодня измеряется как 1 к 6900; ее немного и это хорошо, так как в целом она действует на организмы угнетающе (подробнее рассмотрим этот вопрос ниже).
История открытия
Впервые ее молекулы в обычной среде обнаружил американский физиохимик Гарольд Юри: было это в 1932-м году, а в 1934-м ему присудили Нобелевскую премию за это открытие. В 1933-м уже другой ученый из США, Гилберт Льюис, путем электролиза получил чистую тяжеловодородную воду: он многократно пропускал ток через остаток H2O, постепенно насыщая его молекулами HDO и D2O – до тех пор, пока концентрация последних не достигла 99%.
Когда в 1938-м открыли деление ядер, сразу же стало ясно, насколько перспективны цепные реакции этого процесса. Но для их проведения понадобился эффективный замедлитель нейтронов. В роли последнего стали использовать D2O — наиболее удобное с технической точки зрения соединение дейтерия, помимо прочего, еще и отводящее тепло из рабочей зоны.
В СССР химическая формула тяжелой воды и те преимущества, которые она дает, получала все больше внимания по мере развития атомной энергетики. В частности, предшественница ИТЭФ, Лаборатория №3 АН СССР, начала производить 2H2O в промышленных масштабах – для обеспечения нужд реакторов (современная классификация которых – тип PHWR) и различных установок.
Физические свойства тяжелой воды
Одни из них такие же, что и у обычной, другие — кардинально отличаются, но общая их совокупность определяет условия применения и употребления D2O (2H2O), а значит заслуживает внимания. Рассмотрим каждый из важных параметров отдельно.
Запах
Отсутствует — по этому показателю отличить ее от «легкой» не представляется возможным. Какие-то оттенки неприятного аромата — допустим, серной тухлости, хлористой резкости или гниловатой сладости — говорят только о наличии вполне конкретных проблем в самом источнике, вызванных не превышением концентрации оксида дейтерия. Причина может быть в разложении водорослей, сливе промышленных отходов и других подобных факторах.
Во всех вариациях своих изотопов тяжелая вода в природе так же прозрачна, как обычная. Поэтому вполне можно спутать ее визуально и случайно выпить, если она, например, будет налита в стакан или графин (на вкус она может показаться чуть сладковатой).
Обратите внимание: помутнение, затемнение или осветление, появление буроватого или зеленоватого оттенка свидетельствует лишь о присутствии примесей в отдельно взятом заборе, но никак не о повышенном содержании D2O, его так просто не определить. Другой вопрос, чем обусловлено наличие посторонних веществ (чаще всего это соли жесткости, ржавчина, нитраты, марганец и другие опасные элементы).
Температура кипения
Это первое свойство, по которому тяжелая вода будет отличаться от легкой, пусть и незначительно. Потому что при сравнении мы увидим следующие градусы:
MBFT-75 Мембрана на 75GPD
SF-mix Clack до 0,8 м3/ч
SF-mix Runxin до 0,8 м3/ч
Нагрев является своеобразным маркером «веса», но в условиях бытовой практики он малоприменим, а наука и промышленность располагают более совершенными и точными способами определения разницы.
Отдельно отметим, что выделяют еще и такой показатель, как температура плавления (кристаллизации), и он составляет:
Проще говоря, это отметка, при которой начинает образовываться лед, и это даже более явный признак «тяжести», который может пригодиться в быту.
Вязкость
Имеется в виду динамическая, являющаяся частью системы единиц СГС и измеряемая в сантипуазах (сокращенно сП). При этом 1 П = 0,1 Н х с/м2.
У обычной она 1,0016 сП, в то время как у оксида дейтерия уже 1,2467 сП (все сравнения производятся при температуре в 20 градусов Цельсия). Разница в 24% существенным образом влияет на эксплуатационные характеристики и является одним из тех факторов, которые способствуют замедлению химических реакций (в частности, поглощения нейтронов).
Молекулярная масса
Составляет 20,034 г/моль, по сравнению с 18,01528 г/моль «легкой» H2O, и это еще одна из причин, почему воду называют тяжелой, ведь она буквально весит больше. Данная особенность также провоцирует снижение скоростей обменных процессов, что особенно важно для управления термоядерным синтезом.
Растворимость
Она достаточно быстро и равномерно смешивается с этанолом, но в случае с диэтиловым эфиром такого результата уже не наблюдается. В свою очередь, растворить в ней соли уже значительно труднее, чем в обычной H2O, ориентированной на бытовые нужды, и это даже удобно. Во-первых, это явный показатель повышенного «веса», во-вторых, определенная защита от загрязнений, что просто необходимо технологической среде, актуальной на самых ответственных объектах.
Плотность
Измеряется при температуре в 25 градусов Цельсия и составляет 1,1042 г/см3, по сравнению с 0,997 г/см3 «легкой». И это еще одна характеристика, снижающая общий уровень поглощения нейтронов и способствующая замедлению реакций.
Есть и другие параметры, в числе которых:
Но они не столь важны конкретно в нашем случае, то есть в вопросах подготовки забора из артезианской скважины к бытовому употреблению, и поэтому на каждом из них мы не будем подробно останавливаться.
Где и для чего используется тяжелая вода
Поначалу сам Гарольд Юри отнесся к своей находке как к интересному научному факту. И, несмотря на Нобелевскую премию, на первых порах он и его коллеги не видели сфер, в которых может пригодиться оксид дейтерия. Ситуация изменилась уже через 5 лет: в связи с открытием деления ядер, стал очевиден тот промышленный потенциал, которым обладает D2O. В результате сегодня можно выделить сразу несколько сфер ее актуальности.
В ядерных технологиях
SF-mix ручной до 0,8 м3/ч
Аэрационная установка AS-1054 VO-90
Современные физики рассматривают ее в качестве топлива будущего, а некоторые даже заявляют, что она станет источником бесконечной энергии. И это уже не просто мечты, ведь с ее помощью уже можно управлять термоядерным синтезом (пусть пока и с ограничениями), и ожидается, что с ее помощью удастся провести сверхвыгодные реакции вроде:
D + T → 4He + η + 17,6 МэВ
Перспективность считается настолько высокой, что ее коммерческий оборот в ряде стран находится под жестким государственным надзором. Это как раз та ситуация, в которой запреты и ограничения оправданы, так как позволяют защититься от создания неконтролируемых, а значит и опасных установок, работающих на природном уране.
Важную роль играет и возможность обнаружения нейтрино именно с помощью D2O. Около 1000 ее тонн содержится в SNO, то есть в крупнейшем детекторе мира, комплексе оборудования, расположенном в Канаде.
В ядерных реакторах
В этом случае применение тяжелой воды актуально в одном из двух качеств:
В роли изотопного индикатора в химии
А также в области гидрологии, биологии и других сферах, для которых только может быть актуальным использование оксида дейтерия.
Например, в небольших концентрациях он препятствует размножению и распространению бактерий, грибков и других вредных микроорганизмов, и эту особенность взяла на вооружение экспериментальная медицина.
Рассуждая о том, что такое тяжелая вода и где применяется, нужно отметить, что ученые в течение десятилетий проводили глобальные и комплексные исследования. И установили несколько любопытных закономерностей, возникающих при определенном проценте содержания D2O в употребляемой в пищу жидкости:
Естественно, все медицинские опыты (тем более что они показывают столь неоднозначные результаты) пока проводились на животных, но не на людях.
Отличия между легкой и тяжелой водой
На основании свойств D2O понятно, чем опасно такое соединение для человека: постепенно накапливаясь в организме, оно нарушает метаболизм, убыстряет появление необратимых возрастных изменений, провоцирует возникновение болезней и злокачественных новообразований.
С другой стороны, H2O, с нормальной или восстановленной структурой:
Напомним также, что обе этих жидкости прозрачны и обладают нейтральным вкусом и запахом, поэтому их вполне реально перепутать.
Какая польза от тяжелой воды
Диспенсер магистральный настольный AquaPro 919H/RO (горячая и холодная вода)
Диспенсер магистральный настольный AquaPro 929CH/RO (охлаждение/нагрев)
Диспенсер напольный AquaPro 311 (пустой, без охлаждения)
Естественно, она не была столь востребованной, если бы несла только вред. То же замедление нейтронов обеспечивает нормальное протекание ядерных реакций, а значит оксид дейтерия все-таки стоит на страже нашей безопасности, пусть и опосредованно.
Ну а добавление в качестве индикатора дает удобную возможность контролировать изменения состава смесей и своевременно вносить необходимые корректировки.
Также нужно учитывать те потенциальные преимущества, которые в будущем принесут медицинские исследования. Специалисты из самых разных областей все уверенней говорят о скором прорыве.
Что случится, если выпить тяжелую воду
В небольших количествах она никак не скажется на состоянии организма. За раз можно употребить даже литр D2O — ничего страшного не случится: за две недели она полностью выйдет из тела, а сам дейтерий не радиоактивен. Так что не опасайтесь, что случайно возьмете не тем наполненный стакан. Максимум, что можно почувствовать — это небольшой дискомфорт из-за изменения давления.
Другое дело — регулярное употребление. В этом случае оксид будет:
Это обернется уже описанными проблемами со здоровьем (отказом органов, появлением опухолей). Если же концентрация D2O достигнет 20% от общего объема жидкости, то это спровоцирует летальный исход.
Тяжелая вода в жизни человека
За тот комплексный угнетающий эффект, который она может подарить, ее зачастую называют мертвой. Да, несмотря на то что размножение вредных микроорганизмов она тоже замедляет или даже полностью останавливает.
Нюанс в том, что оксид дейтерия в малых количествах, но содержится во всех естественных источниках. Небольшой его процент есть в озерах, прудах, реках, морях, глубоких скважинах и даже в осадках. Причем в дожде его обычно в несколько раз больше, чем в снеге, что объясняется частой электризацией облаков.
В любом случае выходит, что мы, пусть и неосознанно, но потребляем D2O, и получение тяжелой воды в домашних условиях происходит независимо от нашего желания, просто не в таких количествах, которые могли бы нам навредить.
Поэтому важно не повышать риск накопления оксида дейтерия в организме и не употреблять для питья и приготовления пищи морскую H2O, опресненную методом обратного осмоса. Данный способ как раз даст жидкость со сравнительно более высоким уровнем концентрации изотопа.
Мы поможем подобрать оборудование, которое будет контролировать количество примесей в каждом заборе и отфильтровывать вредные частицы – обращайтесь в компанию «Вода Отечества».
Но механическая очистка в этом конкретном случае может не сработать, так как фильтры смогут удалить лишь нерастворимые частицы, но окажутся бессильными на уровне молекул и атомов. Хотя один способ, применимый в быту, все-таки есть, предлагаем его рассмотреть.
Как получить тяжелую воду в домашних условиях
Выделить D2O, чтобы потом слить его, можно с помощью процесса таяния. Для этого необходимо:
Заключение
Теперь вы знаете, что означает понятие «тяжелая вода», где она может применяться и какую опасность несет, и еще больше понимаете, насколько важно получать во всех смыслах чистую жидкость.