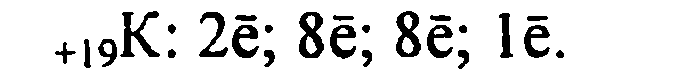Неметаллические свойства фосфора выражены ярче чем у элементов азота
У каких из приведенных элементов наиболее ярко выражены неме- таллические свойства: у фосфора, алюминия, кремния, серы,
Ответ или решение 2
В данной задаче Вам нужно определить, у какого вещества наиболее ярко выражены неметаллические свойства. Для того, чтобы решить ее, воспользуемся периодической системой элементов Д.И.Менделеева.
Изменение неметаллических свойств в периоде
Обратим внимание на то, что алюминий, кремний, фосфор и хлор находятся в одном периоде.
Как известно, в периоде неметаллические свойства усиливаются слева направо.
Изменение неметаллических свойств в группе
Но мы совсем забыли про фтор, который благополучно оставили в другом периоде и совсем не стали рассматривать.
Нельзя забывать о том, что в группах неметаллические свойства усиливаются снизу вверх. А так как фтор выше, чем хлор, то фтор и будет тем элементом, у которого наиболее ярко выражены неметаллические свойства.
Ответить на данный вопрос нам поможет периодическая система. Неметаллические свойства элементов увеличиваются:
1) в периодах — слева направо;
2) в группах — снизу вверх.
Запомнить легко, если ориентироваться на фтор (F) — он самый активный неметалл.
Расположим данные элементы в порядке увеличения их неметаллических свойств:
Химия
А Вы уже инвестируете?
Слышали про акцию в подарок?
Зарегистрируйся по этой ссылке
и получи акцию до 100.000 руб
План урока:
Азот и фосфор
Азот находится под номером 7 в периодической системе, соответственно и заряд ядра его равен +7. Атомный вес равен 14,007 а.е.м. Неметалл, второй период, V группа A подгруппа.
Азот — простое вещество. В природе азот – двухатомная молекула N2 (представлена ниже). Отличительная черта молекулы этого элемента — это связь ее атомов через очень прочную ковалентную связь.
Строение атома азота Источник
Строение атома фосфора Источник
На данный момент известно, что данное вещество способно на аллотропию 11 раз, именно столько модификаций есть в природе данного элемента. Наиболее распространены три (или можно объединить их в три группы): черный, белый и красный. О них будет речь ниже.
Аллотропия фосфора
Наибольшее распространение получил фосфор белый, из-за примесей иногда бывает желтого цвета. Молекулярная решетка, составлена четырьмя атомами фосфора.
Вещество быстро вступает в реакции, пластилинообразное на ощупь, неприятное на запах, с нотками чеснока. Цвета бледновато желтого. Растворим в сероуглероде и бензоле, но не в воде. В реакции с паром H2O получаем смесь из газов. Токсично, возгорается в процессе трения. Светится в темноте. Плавится при 44 градусах. Особые условия хранения, ввиду активности вещества хранят под слоем воды.
Красный фосфор — разновидность фосфора, цветовая гамма которых расположилась от оранжевого до фиолетового спектра. Плотность так же различна, как и окрас. За образование красного фосфора ответственен белый фосфор, но нагретый порядком до 320 °С без кислорода. Дальнейшее нагревание до 560 °С кристаллизует и увеличивает температуру, при которой красный фосфор будет плавиться, попутно уменьшая реакционную способность. Исходя из выше написанного мы можем считать, что эта модификация фосфора менее активна белого фосфора. Не растворимо в воде и в сероуглероде. Безвредно, но и в темноте не светится.
Следующая модификация фосфора (черная) добывают из белого, нагревая последний до 230 °С и повышая давление. Наиболее стабильная форма. Имеет три разновидности: ромбическую, кубическую и гексагональную. Отличие разновидностей в строении молекулярной решетки.
Эта разновидность фосфора по внешним особенностям больше похожа на металл, об этом говорит его блеск и наличие свойств электро- и теплопроводности. Почти инертен, не вступает в реакцию даже с растворителями органического рода, твердый на ощупь.
Основные соединения азота и фосфора
Основные соединения азота
Получение аммиака:
3H2 + N2 → 2NH3 + Q, необходимы условия для стабилизации реакции и для наибольшего выхода: давление от 15 до 100 Мпа и катализаторы.
Аммиак. Водный раствор (нашатырный спирт)
Получение аммиака в лаборатории возможно путем взаимодействия гашеной извести и твердого хлорида аммония (NH4Cl). При этом необходимо смесь нагревать.
Свойства аммиака
Оксиды азота
Азот выделяется среди других элементов большим количеством оксидов. Его оксиды термодинамически неустойчивы к распаду на простые вещества. Но при 700 °С реакция разложения оксидов кинетически заторможена. О них будет идти речь ниже.
Азотистая кислота. Формула HNO2
Нитрат аммония (аммонийная селитра) NH4NO3. Продукт взаимодействия азотной кислоты с NH4OH (гидрат аммиака). Первооткрывателем вещества является Иоганн Глаубер. Открыто вещество в 1659 году. Применяется как компонент взрывчатых веществ и удобрение.
Минеральные удобрения — это группа неорганических соединений, питающие растения элементами в виде минеральных солей различного рода. Активно применяется в Агро промышленности.
Взаимодействие азотной кислоты с металлами и неметаллами
Взаимодействие с металлами
При этом есть одна закономерность в реакциях азотной кислоты и металлов: чем менее концентрирована азотная кислота и более активен метал, тем больше происходит восстановление азота:
Реакции с металлами протекают по окислительно-восстановительному механизму, коэффициенты в уравнениях реакций могут быть определены методом электронного баланса.
Пример
Взаимодействие концентрированной азотной кислоты с медью.
Обобщенные особенности взаимодействия азотной кислоты с металлами можно выделить следующие:
Краткая схема протекания реакции азотной кислоты с металлами: Металл + НNO3 ↔ вода + нитрат + газ
Основные соединения фосфора
Фосфор достаточно активный элемент и образует большое количество оксидов, среди них можно выделить два. Наиболее важные: оксид фосфора (III) P2O3 и оксид фосфора (V) P2O5.
Первый оксид называют иначе фосфористым ангидридом (P2O3). Получают при медленном сжигании фосфора в бескислородной среде.
В нормальном состоянии представляет собой белую массу, состоящую из хлопьев или кристаллов. Токсичен. Очень летучий. На свету сначала желтеет, потом краснеет. Хорошая растворимость в органических растворителях (в бензоле и сероуглероде). По своей природе оксид кислотный.
Подвергается окислению кислородом, образуя наш следующий оксид (Р2О5):
Оксид фосфора (V) – фосфорный ангидрид. При нормальных условиях представлен в виде белого влагопоглощающего порошка. Из-за влагопоглощающих свойств, хранение осуществляется в плотно закрытых сосудах. Наиболее часто применяют свойство влагопоглощения при осушении газов и жидкостей. Получают, как указано в предыдущей реакции, окислением оксида выше или же сжиганием фосфора в избытке кислорода:
Оксид по своей природе кислотный, и соответственно осуществляет взаимодействие с водой, оксидами основной природы и щелочами:
Р2О5 + Н2О →2HPO3 при температуре 0°С образуется метафосфорная кислота
Р2О5 + 6NaOH →ЗН2О + 2Na3PO4(ортофосфат натрия, средняя соль)
Р2О5 + 4NaOH →Н2О + 2Na2HPO4(гидрофосфа́т на́трия, кислая соль)
Р2О5 + 2NaOH →Н2О + 2NaH2PO4(дигидрофосфат натрия, кислая соль)
Фосфорные кислоты
Получение фосфорной кислоты:
Химические свойства азота и фосфора
Химические свойства азота
Тройная связь влияет на активность азота. Соединения азота разлагаются легко, при нагревании образуются свободный азот.
Химические свойства фосфор
Реакционная способность наивысшая у белого фосфора и наименьшая у черного, почти инертен. Ясно иллюстрируется градация активности, зависящая от модификации.
При этом фосфор имеет большую реакционную способность. Это распространяется как на простые, так и на сложные вещества.
Соединения фосфора с кислородом прочнее таковых соединений с азотом. Это происходит из-за того, что неметаллические свойства фосфора слабее, чем неметаллические свойства азота.
У какого элемента ярче выражены неметаллические свойства у азота или фосфора
Б) Характеристика калия.
1. Калий имеет порядковый номер 19, Z = 19 и относительную атомную массу Аr(К) = 39. Соответственно заряд ядра его атома +19 (равен числу протонов). Следовательно, число нейтронов в ядре равно 20. Так как атом электронейтрален, то число электронов, содержащихся в атоме калия, тоже равно 19. Элемент калий находится в четвертом периоде периодической системы, значит, все электроны располагаются на четырех энергетических уровнях. Таким образом, строение атома калия записывается так:
Исходя из строения атома, можно предсказать степень окисления
калия в его соединениях. Так как в химических реакциях атом калия отдает один внешний электрон, проявляя восстановительные свойства, следовательно, он приобретает степень окисления +1.
Восстановительные свойства у калия выражены сильнее, чем у на-
трия, но слабее, чем у рубидия, что связано с ростом радиусов от Na к Rb.
2. Калий— простое вещество, для него характерна металлическая
кристаллическая решетка и металлическая химическая связь, а отсюда — и все типичные для металлов свойства.
3. Металлические свойства у калия выражены сильнее, чем у на-
трия, но слабее, чем у рубидия, т.к. атом калия легче отдает электрон, чем атом натрия, но труднее, чем атом рубидия.
4. Металлические свойства у калия выражены сильнее, чем у кальция, т.к. один электрон атома калия легче оторвать, чем два электрона
атома кальция.
5. Оксид калия К2O является основным оксидом и проявляет все типичные свойства основных оксидов. Взаимодействие с кислотами и кислотными оксидами.
К2O + 2НСl = 2КСl +Н2O; К2O + SO3 = K2SO4.
6. В качестве гидроксида калию соответствует основание (щелочь) КОН, которое проявляет все характерные свойства оснований: взаимодействие с кислотами и кислотными оксидами.
KOH+HNO3 = KNO3+H2O; 2KOH+N2O5 = 2KNO3+H2O.
7. Летучего водородного соединения калий не образует, а образует гидрид калия КН.
Описание презентации по отдельным слайдам:
1 слайд
Описание слайда:
2 слайд
Описание слайда:
Удивить готов он нас – Он и уголь, и алмаз, Он в карандашах сидит, Потому что он — графит. Грамотный народ поймет То, что это … В чем горят дрова и газ, Фосфор, водород, алмаз? Дышит чем любой из нас Каждый миг и каждый час? Без чего мертва природа? Правильно, без … В воздухе он главный газ, Окружает всюду нас. Угасает жизнь растений Без него, без удобрений. В наших клеточках живет Важный элемент … КИСЛОРОДА АЗОТ УГЛЕРОД
3 слайд
Описание слайда:
4 слайд
Описание слайда:
5 слайд
Описание слайда:
Кроме того, к неметаллам относят также водород и гелий. Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов: O 1ѕ²2ѕ²2p⁴ Cl 1ѕ²2s²2p⁶3s²3p⁵ Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов.
6 слайд
7 слайд
Описание слайда:
ЗАДАНИЕ: Напишите электронные формулы – серы, фтора, мышьяка, брома S 1s²2s²2p⁶3s²3p⁴ F 1s²2s²2p⁵ As 1s²2s²2p⁶3s²3p⁶4s²4p³ Br 1s²2s²2p⁶3s²3p⁶4s²4p⁵ У какого из элементов ярче выражены неметаллические свойства и почему: а) As – N б) Cl – S а) N – меньше радиус атома (больше значение электроотрицательности) б) Cl – меньше радиус атома, больше валентных электронов ( больше значение ЭО)
8 слайд
Описание слайда:
НАХОЖДЕНИЕ НЕМЕТАЛЛОВ В ПРИРОДЕ В свободном виде могут быть газообразные неметаллические простые вещества — фтор, хлор, кислород, азот, водород, инертные газы, твёрдые — иод, астат, сера, селен, теллур, фосфор, мышьяк, углерод, кремний, бор, при комнатной температуре в жидком состоянии существует бром. Распространёнными являются кислород, кремний, водород; редкими — мышьяк, селен, иод.
9 слайд
10 слайд
Описание слайда:
Чаще неметаллы находятся в химически связанном виде: вода, минералы, горные породы, различные силикаты, фосфаты, сульфиды. силикат натрия сульфид свинца
11 слайд
Описание слайда:
12 слайд
Описание слайда:
а т м о с ф е р а к л е т к а
13 слайд
Описание слайда:
14 слайд
Описание слайда:
15 слайд
Описание слайда:
16 слайд
Описание слайда:
С Е Р А КРАСНЫЙ ФОСФОР БЕЛЫЙ ФОСФОР
17 слайд
Описание слайда:
18 слайд
Описание слайда:
У некоторых неметаллов наблюдается проявление аллотропии: – для газообразного кислорода характерны две аллотропных модификации — кислород (O2) и озон (O3), – для твёрдого углерода множество форм — алмаз, астралены, графен, графан, графит, карбин, фуллерены, стеклоуглерод ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ АЛМАЗ ГРАФИТ
19 слайд
Описание слайда:
20 слайд
Описание слайда:
21 слайд
Описание слайда:
ХИМИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ Окислительные свойства простых веществ: Реагируют с металлами 2K + S⁰ = K₂S⁻² 3Ca + N₂⁰ = Ca₃N₂⁻³ 2Fe + 3 Cl₂⁰ = 2 FeCl⁻₃ Реагируют с водородом H₂ + S⁰ = H₂S⁻² 3N₂⁰ + H₂ = 2N⁻³H₃ Реагируют с неметаллами с более низким значением электроотрицательности 2P⁰ + 5S⁰ = P₂⁺⁵S₅⁻² S⁰ + 3 F₂⁰ = S⁺⁶F₆⁻ Реагируют с некоторыми сложными веществами C⁻⁴H⁺₄ + 2 O⁰₂ = C⁺⁴O₂⁻² + 2 H₂⁺O⁻² 2 KI⁻ + Cl₂⁰ = 2 KCl⁻ + I₂⁰
22 слайд
Описание слайда:
23 слайд
Описание слайда:
Восстановительные свойства неметаллов ( простых веществ): Со фтором все восстановители 2) С кислородом S⁰ + O₂ = S⁺⁴O₂ Si⁰ + O₂ = Si⁺⁴O₂ 4P⁰ + 5O₂ = 2P₂⁺⁵O₅ 3) Со сложными веществами-окислителями Например – H₂, C 3C⁰ + 2Fe₂O₃ = 3C⁺⁴O₂ + 4Fe H₂⁰ + CuO = H₂⁺O + Cu
24 слайд
Описание слайда:
ЗАДАНИЕ Составьте уравнения реакций и определите восстановитель: Si + F₂→ S + H₂SO₄ → SO₂ + … H₂ + WO₃ → Br₂ + H₂S → S + … Li + N₂ → C + HNO₃ → NO₂ + … + … ОТВЕТ: Si + 2F₂ = SiF₄ 3H₂ + WO₃ = 3H₂O + W 6Li + N₂ = 2Li₃N S + 2H₂SO₄ = 3SO₂ + 2H₂O Br₂ + H₂S = S + 2HBr C + 4HNO₃ = CO₂ + 2H₂O+ 4NO₂
25 слайд
Описание слайда:
ПОЛУЧЕНИЕ НЕМЕТАЛЛОВ в промышленности
26 слайд
Описание слайда:
Молекулярный азот в промышленности получают фракционной перегонкой жидкого воздуха. Этим методом можно получить и «атмосферный азот: В промышленности кремний технической чистоты получают, восстанавливая расплав SiO2 коксом при температуре около 1800 °C в руднотермических печах шахтного типа. Чистота полученного таким образом кремния может достигать 99,9 %
27 слайд
Описание слайда:
Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре 1600 °С: Образующиеся пары белого фосфора конденсируются 2Ca₃(PO₄)₂↓+10C+6SiO₂↓=P₄+10CO↑+6CaSiO₃↓ в приёмнике под водой.
28 слайд
Описание слайда:
Хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли: 2NaCl + 2H2О ±2е- → H2↑ + Cl2↑ + 2NaOH
29 слайд
Описание слайда:
Р Е Б У С Ы Й О Д К Р Е М Н И Й
30 слайд
Описание слайда:
А З О Т У Г Л Е Р О Д
31 слайд
Описание слайда:
1. Неметаллы, расположенные в порядке усиления их неметалличности, – это 1) азот, углерод, бор 3) фтор, кислород, хлор 2) сера, хлор, фтор 4) бор, кремний, водород 2. Неметаллические свойства элементов в ряду углерод- азот- кислород-фтор: 1) не изменяются 2) усиливаются 3) ослабевают 4) изменяются периодически Т Е С Т ОТВЕТ: 1 – 2 2 – 2 3 – 4 4 – 3 3.Завершенный внешний энергетический имеет частица: 1) P⁺³ 2) S⁺⁴ 3) Cl⁺⁵ 4) C⁻⁴ 4. Частице Si⁻⁴ соответствует электронная конфигурация: 1) 1s²2s²2p⁶3s² 2) 1s²2s²2p⁶3s²3p⁴ 3) 1s²2s²2p⁶3s²3p⁶4s²
32 слайд
Описание слайда:
33 слайд
Описание слайда:
9. Схеме превращения P⁻³→ P⁺⁵ соответствует уравнение: 1) 4P + 5O₂ = 2P₂O₅ 2) P₂O₅ + 3H₂O = 2H₃PO₄ 3)2PH₃ + 4O₂ = P₂O₅ + 3H₂O 4) P₂O₅ + 6NaOH = 2Na₃PO₄ + 3H₂O ОТВЕТ: 9 – 3 10. Простое вещество сера взаимодействует с каждым из веществ ряда: 1) HCl, Na, O₂ 2) Mg, O₂, H₂ 3) K, Zn, Na₂SO₄ 4) Al, H₂O, O₂ ОТВЕТ: 10 – 2 11. Расставьте коэффициенты в схеме реакции: P + H₂SO₄ → H₃PO₄+ SO₂ + H₂O ОТВЕТ: 2P⁰ + 5H₂S⁺⁶O₄ → 2H₃P⁺⁵O₄+ 5S⁺⁴O₂ + 2H₂O
Выберите книгу со скидкой:
БОЛЕЕ 58 000 КНИГ И ШИРОКИЙ ВЫБОР КАНЦТОВАРОВ! ИНФОЛАВКА
Инфолавка – книжный магазин для педагогов и родителей от проекта «Инфоурок»
Курс повышения квалификации
Курс профессиональной переподготовки
Курс профессиональной переподготовки
Учитель биологии и химии
Найдите материал к любому уроку,
указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Учебник:
«Химия. Базовый уровень», Габриелян О.С.
Наиболее сильными неметаллическими свойствами обладает 1)азот ; 2)фосфор ; 3)углерод ; 4)кремний?
Наиболее сильными неметаллическими свойствами обладает 1)азот ; 2)фосфор ; 3)углерод ; 4)кремний.
Если я не ошибаюсь, то либо кремний, либо фосфор.
Неметаллические свойства фосфора выражены сильнее, чем у C O Cl S?
Неметаллические свойства фосфора выражены сильнее, чем у C O Cl S.
Элемет, имеющий свойства неметаллические 1?
Элемет, имеющий свойства неметаллические 1.
Сравнить неметаллические свойства элементов?
Сравнить неметаллические свойства элементов.
Поставить знаки больше, меньше.
Наиболее ярко выраженные неметаллические свойства проявляют :1)азот2)фосфор3)мышьяк4)кремний?
Наиболее ярко выраженные неметаллические свойства проявляют :
50 баллов даю помогите1)какими свойствами обладает элемент с порядковым номером 18?
50 баллов даю помогите
1)какими свойствами обладает элемент с порядковым номером 18?
2) Какой из элементов C или N обладает более сильными неметаллическими свойствами?
3) как записывается формулы оксида этого элемента?
4)Какой из элементов углерод или кремний обладает более сильными неметаллическими свойствами?
5)Какими свойствами обладает элемент с порядковым номером 10?
6) Какие свойства проявляет элемент с порядковым номером 25?
7)напишите формулы оксида.
У каких из приведенных элементов наиболее ярко выражены неметаллические свойства : у фосфора алюминия кремния серы фтора хлора?
У каких из приведенных элементов наиболее ярко выражены неметаллические свойства : у фосфора алюминия кремния серы фтора хлора.
Неметаллические свойства серы выражены слабее чем неметаллические свойства : 1) хора 2) фосфора 3) магния 4) кремнияОбъяснить почему?
Неметаллические свойства серы выражены слабее чем неметаллические свойства : 1) хора 2) фосфора 3) магния 4) кремния
Неметаллические свойства у азота выражены сильнее, чем у :1)Углерода2)Кислорода3)Фтора4)Хлора?
Неметаллические свойства у азота выражены сильнее, чем у :
У кремния неметаллические свойства выражены сильнее, чем :1)у углерода2)у фосфора3)у германия4)у серы?
У кремния неметаллические свойства выражены сильнее, чем :
А. Основные оксиды могут находится в твёрдом и жидком агрегатном состояние Б. Гидроксидами кислотных оксидов являются кислородсодержащие кислоты. 2)верно только Б.
Задание 30 Надеюсь, что было необходимо такое решение.
HF = H : F BCl = B : Cl C : O вот помоиму.
4 делим на молекулярную массу гидроксида натрия 40 = 0. 1 кл вщ.
Во вложении ___________.