Неспецифические очаги пма по ходу ободочной сигмовидной и прямой кишки что это
Перитонеальный канцероматоз
Перитонеальный канцероматоз
Вам поставили диагноз: перитонеальный канцероматоз (опухоль брюшины)
Предлагаем Вашему вниманию краткий, но очень подробный обзор перитонеального канцероматоза.
Филиалы и отделения, где лечат перитонеальный канцероматоз
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Национальный центр лечения больных канцероматозом
МНИОИ имени П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Руководитель Центра к.м.н. Владимир Михайлович Хомяков – 8 495 150 11 22
Введение
Причины возникновения перитонеального канцероматоза
Развитие перитонеального канцероматоза является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация перитонельного канцероматоза
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация перитонеального канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
Р1 – локальное поражение брюшины
Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы перитонеального канцероматоза
Перитонеальный канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика перитонеального канцероматоза
Перитонельный канцероматоз имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики перитонеального канцероматоза является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии перитонеального канцероматоза без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение перитонеального канцероматоза
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Эффективные подходы к лечению, как правило, подразумевают проведение комбинированной терапии, например, сочетания хирургического вмешательства и системной химиотерапии. Одним из наиболее эффективных методов является локальная химиотерапия. Идея локальной химиотерапии состоит в том, чтобы обеспечить доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Из-за крайне низкой проницаемости этой области для лекарственных препаратов, например, при внутривенном их введении или приеме в виде таблеток, доставка препаратов в виде аэрозоля под давлением углекислого газа даёт накопление препарата в опухоли в значительно больших концентрациях.
Методы лечения перитонеального канцероматоза
Длительное время канцероматоз брюшины и плевры считали терминальной стадией болезни, не подлежащей специальному лечению. Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Гипертермическая интраоперационная внутрибрюшная (внутриплевральная) химиотерапия (HITEC).
Это методика, при которой во время операции в брюшную или плевральную полость вводится подогретый до 42,5С, высококонцентрированный раствор химиотерапевтических препаратов, что обеспечивает их воздействие непосредственно на раковые клетки в брюшной (плевральной) полости при минимальном воздействии на другие органы. Сеанс проводится в течение часа, что позволяет разрушить опухолевые клетки, оставшиеся после так называемой циторедуктивной операции.
Внутрибрюшная (внутриплевральная) аэрозольная химиотерапия под давлением (PIРAC)
Это новейший инновационный метод лечения перитонеального канцероматоза, который обеспечивает доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.
Преимущества лечения перитонеального канцероматоза в МНИОИ имени П.А. Герцена – филиале ФГБУ «НМИЦ радиологии» Минздрава России
Неспецифические очаги пма по ходу ободочной сигмовидной и прямой кишки что это
Исследование «всего тела» заключается в сканировании пациента от уха до верхней трети бедра. Т.е. в область исследования будут включены голова (частично, от козелка уха, без захвата головного мозга), шея, органы грудной полости, брюшной полости, малого таза и костная система (без верхних и нижних конечностей).
Сканирование нижних конечностей проводится за дополнительную плату.
Вопрос №2. Что такое радиофармпрепарат?
Радиофармпрепарат (РФП) – это соединение, состоящее из специального вещества и радионуклида (изотопа, радионуклидной метки). Специальное вещество отвечает за то, в каком органе накопится РФП, а радионуклидная метка позволяет врачу-диагносту увидеть это накопление на изображении.
В настоящее время для производства РФП используется очень широкий спектр как специальных веществ, так и радионуклидных меток. Во всем мире самым часто используемым у онкологических больных соединением специального вещества и радионуклидной метки является 18 F-фтордезоксиглюкоза ( 18 F-ФДГ). В данном соединении 18 F выполняет функцию радионуклидной метки, ФДГ – специального вещества.
Вопрос №3. Что такое физиологическое накопление РФП?
Физиологическое накопление (гиперфиксация) РФП – это повышенное накопление РФП, определяющееся в различных органах и системах в норме.
Физиологическое накопление наблюдается при исследованиях со всеми РФП: 18 F-ФДГ, 11 С-холином, 11 С-метионином, 68 Ga-ПСМА и т.д. В зависимости от типа РФП меняется лишь местоположение физиологической гиперфиксации. Например, при ПЭТ и ПЭТ/КТ с самой часто используемой 18 F-ФДГ физиологическое накопление РФП определяется в коре головного мозга, ротоглотке, носоглотке, мышцах гортаноглотки, миокарде левого желудочка, чашечно-лоханочных системах почек, фрагментарно по ходу петель толстой кишки, мочевом пузыре.
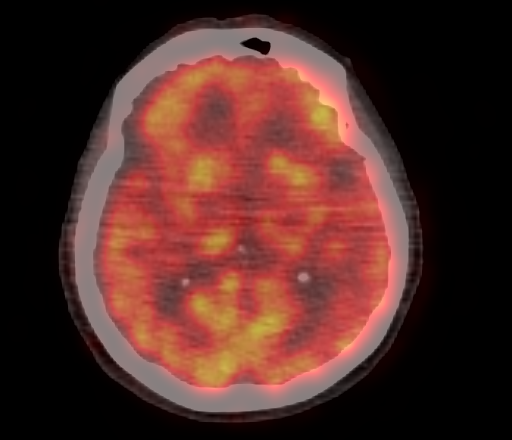 |  |
| Физиологическое накопление 18 F-ФДГ в коре головного мозга. | |
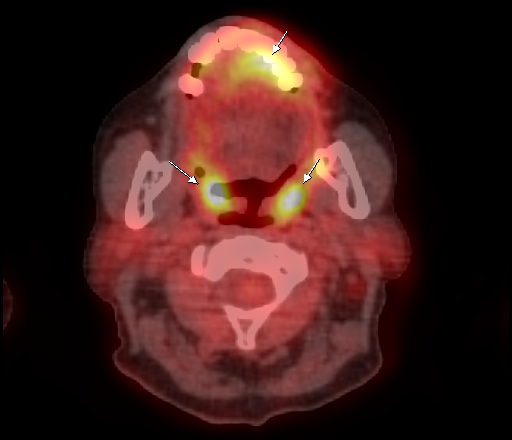 | 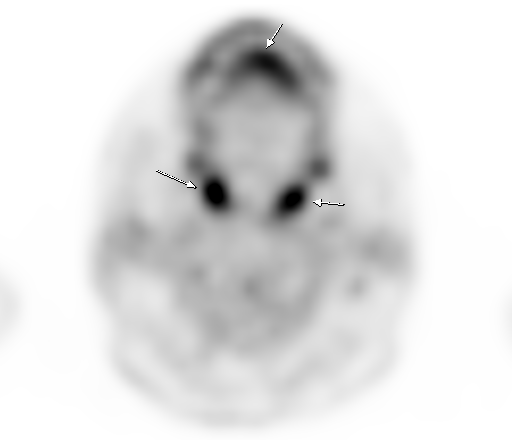 |
| Физиологическое накопление 18 F-ФДГ в ротоглотке. | |
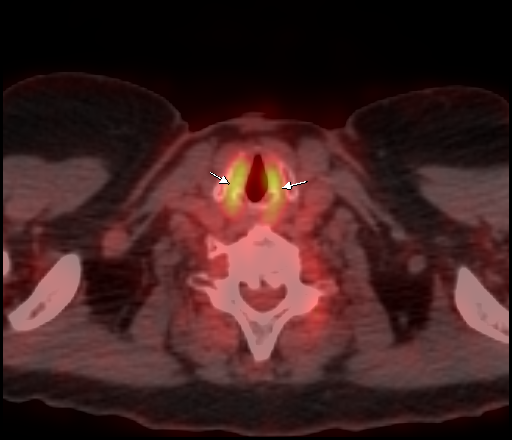 | 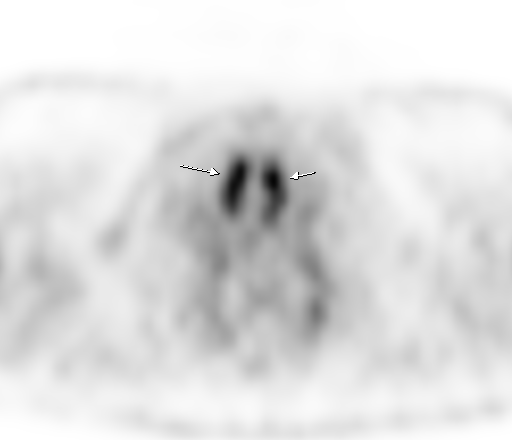 |
| Физиологическое накопление 18 F-ФДГ в мышцах гортаноглотки. | |
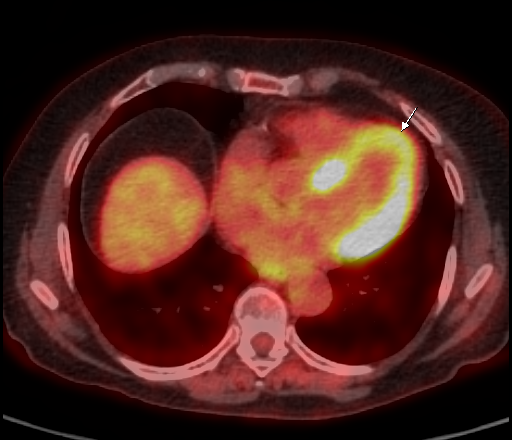 | 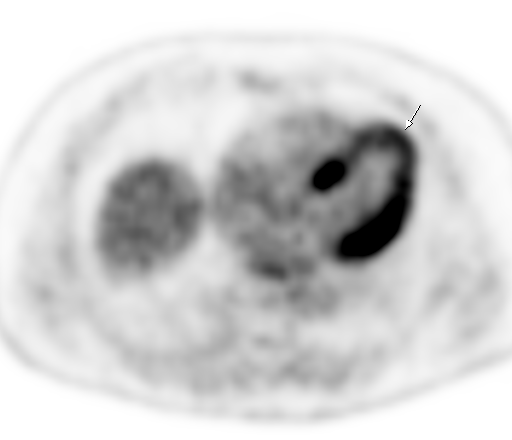 |
| Физиологическое накопление 18 F-ФДГ в миокарде левого желудочка. | |
 |  |
| Физиологическое накопление 18 F-ФДГ в чашечно-лоханочных системах почек. | |
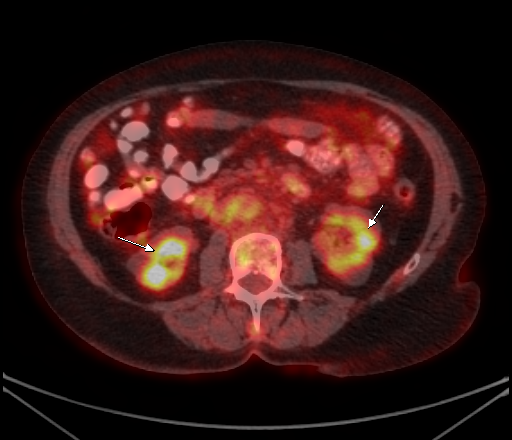
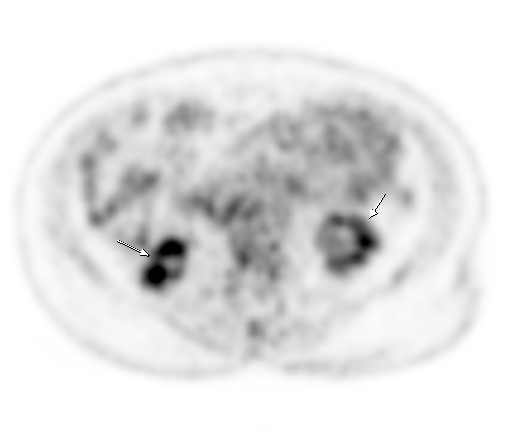
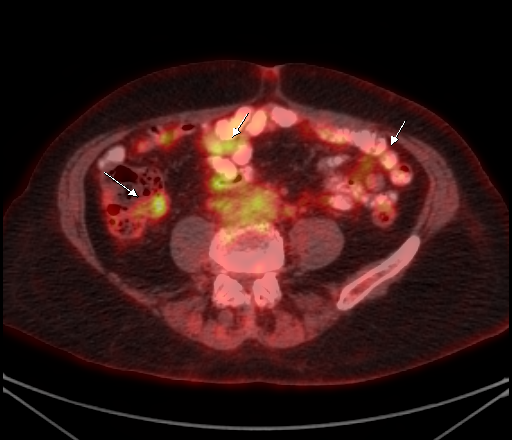 | 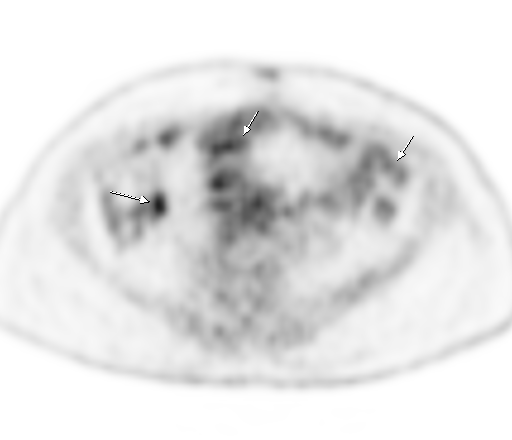 |
| Физиологическое накопление 18 F-ФДГ по ходу петель толстой кишки. | |
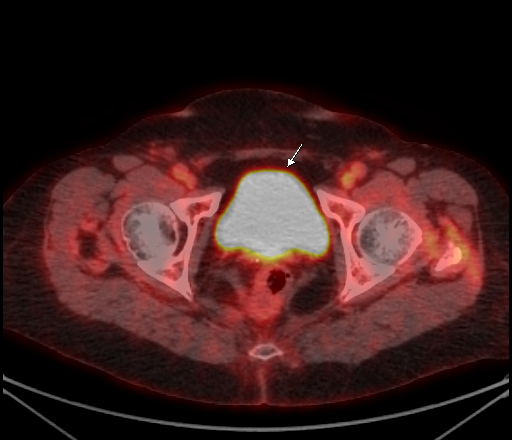 | 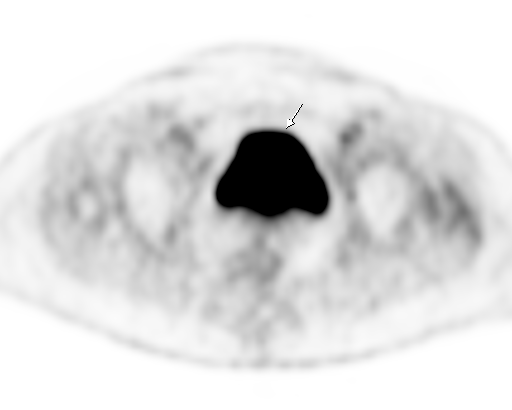 |
| Физиологическое накопление 18 F-ФДГ в мочевом пузыре. | |
Вопрос №4. Что такое патологическое накопление РФП?
Патологическое накопление РФП – это повышенное накопление РФП в органах и тканях, регистрирующееся при заболеваниях, чаще всего в злокачественных опухолях.
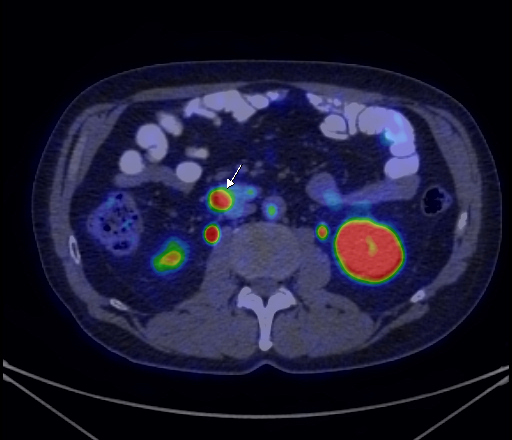 |
| Данные ПЭТ/КТ с 68 Ga-DOTA-TATE у пациента с нейроэндокринной опухолью тощей кишки. В проекции злокачественной опухоли, расположенной в тощей кишке, определяется очаг патологической гиперфиксации РФП. |
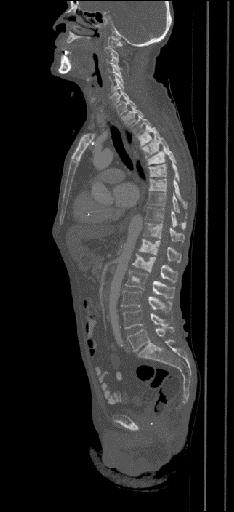 | 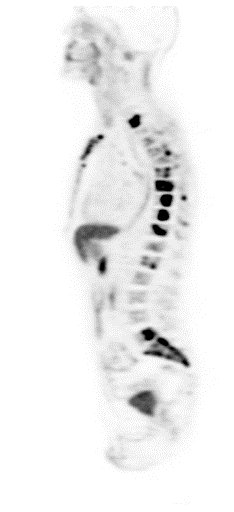 | 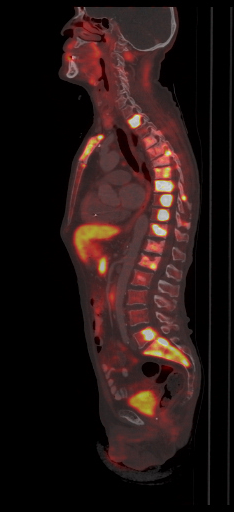 |
| Данные ПЭТ/КТ с 11 С-холином у пациента с раком предстательной железы. Состояние после простатэктомии. В костях скелета визуализируются множественные очаги патологического накопления РФП (метастазы). | ||
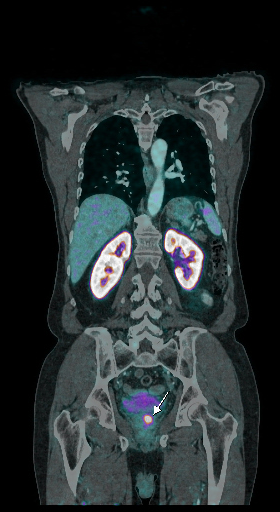 | 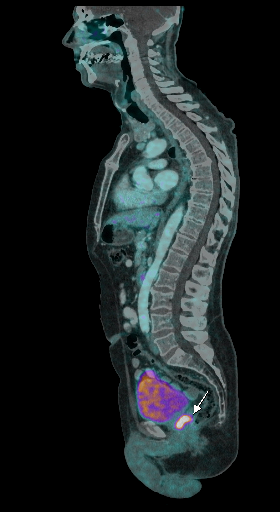 | 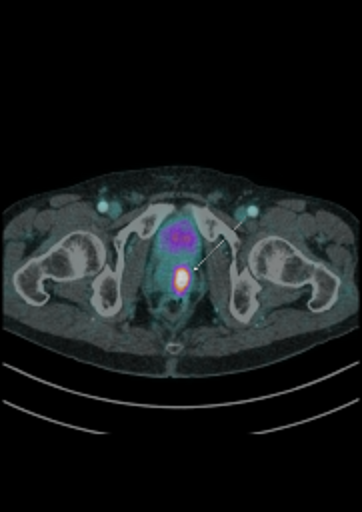 |
| Данные ПЭТ/КТ с 68 Ga-ПСМА у пациента с местным рецидивом рака предстательной железы. Состояние после лучевой терапии. В левых отделах предстательной железы определяется очаг патологического накопления РФП. | ||
Вопрос №5. Что такое метаболически активное и метаболически неактивное образование?
Метаболически неактивное образование – это образование, которое не накопило РФП. Чаще всего отсутствие повышенного накопления РФП в опухоли свидетельствует о ее доброкачественной природе.
Метаболически активное образование – это образование, в котором накопился РФП в повышенном количестве. Повышенное накопление РФП в опухоли чаще всего свидетельствует о ее злокачественном характере.
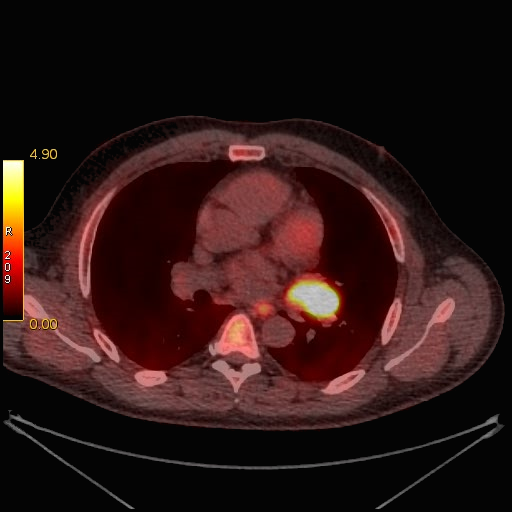 |
| Данные ПЭТ/КТ с 11 С-метионином у больного с метаболически активным образованием корня левого легкого (типичный карциноид). |
Вопрос №6. Что такое SUV?
SUV (Standardized Uptake Value, стандартизированный уровень захвата) – это величина, отражающая интенсивность накопления РФП в зоне интереса, например, в опухоли.
Показатель SUV рассчитывается программным комплексом автоматически и измеряется в различных единицах. В нашем Центре, как и в большинстве отечественных и зарубежных медицинских учреждений, где проводится позитронная эмиссионная томография, в качестве единиц измерения показателя SUV принято использовать г/мл (g/ml).
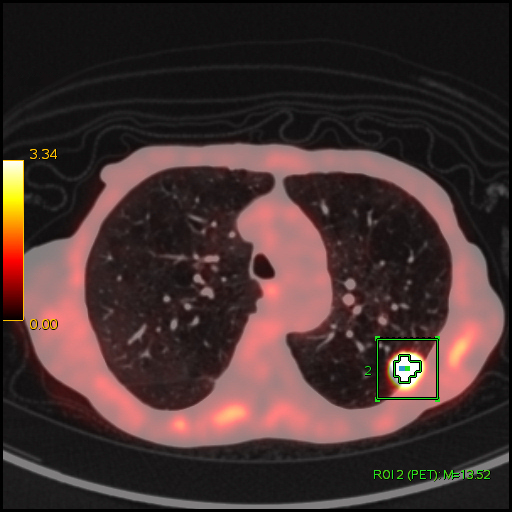 |
| Данные ПЭТ/КТ с 18 F-ФДГ. Оконтуривание метаболически активной злокачественной опухоли левого легкого для измерения показателя SUV. В данном случае величина SUV в опухоли определяется на уровне 13,52 g/ml. |
Вопрос №7. Для чего используется величина SUV?
Величина SUV в основном используется для оценки ответа злокачественной опухоли на проведенное лечение. Важно подчеркнуть, что в ряде клинических ситуаций показатель SUV в опухоли является единственным критерием, позволяющим оперативно получить информацию о чувствительности образования к только что начатой терапии.
Если опухоль чувствительна к лечению, то уровень SUV в ней при повторном ПЭТ-исследовании будет снижаться, если нечувствительна или малочувствительна (резистентна, устойчива) – значение SUV останется без изменений или увеличится. Следует помнить, что своевременная диагностика устойчивости опухоли к лечению позволит скорректировать план лечения, а в некоторых случаях и радикально его изменить.
Как уже было сказано выше, для оценки эффективности терапии врач-радиолог оценивает динамику показателя SUV до и после лечения.
Существует четыре варианта метаболического ответа опухоли на проведенное лечение:
Результаты ПЭТ с 18 F-ФДГ у пациента с диффузной В-клеточной крупноклеточной лимфомой до лечения (а), после 2 курса ПХТ (б) и через 13 месяцев после окончания терапии (в).
а – до лечения в средостении визуализируется массивное метаболически активное образование с уровнем SUV=12,6;
б – после 4 курса ПХТ отмечается значительное уменьшение метаболического объема опухоли и снижение показателя SUV до 3,4 (достигнут частичный метаболический ответ, т.е. опухоль чувствительна к выбранной ПХТ);
в – через 13 месяцев после окончания ПХТ очагов патологической гиперфиксации РФП в проекции органов средостения не обнаружено (достигнут полный метаболический ответ).
Рак ободочной кишки
Анатомия ободочной кишки
Как известно, у человека есть два круга кровообращения – малый (легочный), где происходит получение кислорода и отдача углекислого газа, и большой, в ходе которого кровоснабжаются все органы, а центром, где объединяются эти круги, является сердце. По артериям большого круга кровообращения течет кровь, получившая в легких кислород, от сердца к органам. Правая половина ободочной кишки, как и тонкая кишка, получает кровь из верхней брыжеечной артерии, а левая половина ободочной кишки и верхний отдел прямой кишки – из нижней брыжеечной артерии. Эти артерии являются крупными сосудами, их диаметр может достигать 5-10 мм. Венозная кровь, несущая углекислый газ и продукты обмена веществ, оттекает от толстой кишки по верхней брыжеечной и нижней брыжеечной венам и, прежде чем попасть в сердце и легкие, проходит через печень.
Кто защищает наш организм изнутри?
Лимфатическая система в периоде внутриутробного развития закладывается вместе с артериальной, поэтому лимфатические узлы располагаются у человека вдоль артерий. Для ободочной кишки существует три уровня, или порядка, лимфатических узлов. Лимфоузлы первого порядка находятся у самого края кишки, ближе других к кишечной стенке. Узлы второго и третьего порядка находятся чуть дальше второго порядка – вдоль сосудов среднего калибра, кровоснабжающих кишку, а апикальные (от слова apex (лат.) – верхушка, вершина, apicalis (лат.) — верхушечный), или по-другому лимфатические узлы третьего порядка – у самых крупных сосудов, питающих ободочную кишку. Лимфатические узлы являются «сторожами» организма, защищающими его от распространения чужеродных инфекционных агентов и опухолевых клеток.
Что такое рак ободочной кишки?
Рак (cancer (лат.), c-r) – злокачественная опухоль из эпителиальных клеток, обладающая способностью прорастать в орган и окружающие структуры и распространяться (метастазировать) в лимфатические узлы и другие, расположенные далеко от опухоли, органы. Пациенты нередко называют раком все злокачественные опухоли, хотя это некорректно с точки зрения онкологии.
Рак ободочной кишки развивается из слизистой оболочки стенки кишки, которая и является железистым эпителием. Такая опухоль называется «аденокарцинома» (от aden (лат.) железа и carcinoma (лат.) рак, раковая опухоль). Лечением этого заболевания занимаются врачи-онкологи, колопроктологи, хирурги, химиотерапевты. Опухоли другой природы (карциноид, гастро-интестинальные стромальные опухоли) в толстой кишке встречаются намного реже (3-5% от всех злокачественных новообразований толстой кишки).
В Клинике колопроктологии и малоинвазивной хирургии возможно лечение любых опухолей толстой кишки.
Причины и факторы риска развития рака ободочной кишки
Основным путем развития рака ободочной кишки является злокачественное перерождение полипов – доброкачественных образований слизистой ободочной кишки. Также к факторам риска можно отнести воспалительные заболевания кишечника, нарушения диеты, курение, отягощенный по онкологическим заболеваниям наследственный анамнез.
Большую роль в развитии рака может играть наследственность, так как каждый десятый носитель колоректального рака имеет наследственную предрасположенность к этому заболеванию. Если в вашем роду были родственники с заболеванием колоректальный рак, то следует быть особенно настороженным относительно своего здоровья. Наследственные формы рака могут проявляться даже в раннем возрасте. В такой ситуации особенно важно тщательно и своевременно обследоваться.
Профилактика рака ободочной кишки
Самым эффективным методом профилактики рака ободочной кишки является своевременное удаление полипов. Это малоинвазивная хирургическая операция, выполняющаяся во время колоноскопии – эндоскопического обследования толстой кишки. Для того, чтобы вовремя выявить полипы, зачастую не проявляющие себя никакими симптомами, необходимо, начиная с 45-50-летнего возраста, каждые 5 лет проходить колоноскопию. Людям, чьи родственники болели раком ободочной или прямой кишки, обследование надо начинать проходить в более раннем возрасте, а при установлении диагноза «наследственный колоректальный рак» родственникам пациента необходимо начинать обследование в возрасте на 5 лет младше возраста установки диагноза у заболевшего родственника. Никакие другие методы (онкомаркеры, анализ кала на скрытую кровь, виртуальная колоноскопия) не обладают такой результативностью, как проведение колоноскопии в качестве метода профилактики рака ободочной кишки.
К другим способам профилактики рака ободочной кишки относят диету с ограничением красного мяса и сильно жареной пищи, ограничение употребления алкоголя и курения, поддержание нормального веса тела и активный образ жизни.
Симптомы рака ободочной кишки
«Острые» симптомы рака ободочной кишки являются жизнеугрожающими, вызываются осложнениями рака ободочной кишки и зачастую приводят к экстренной госпитализации в хирургическое отделение на карете скорой медицинской помощи. Следует сказать, что симптомы, о которых пойдет речь в этом разделе, являются характерными не только для осложнений рака ободочной кишки, но и для других экстренных хирургических заболеваний, вызывающих клиническую картину «катастрофы в животе».
Кровотечение из заднего прохода
Выделение крови при дефекации, следы крови на туалетной бумаге и на стенках унитаза сопровождают многие другие, в том числе доброкачественные, колопроктологические заболевания. Поступление из анального отверстия большого количества свежей крови, темных кровяных сгустков или стула, смешанного с кровью, является причиной для экстренного обращения в медицинское учреждение. Причиной кровотечения может быть рак ободочной кишки.
Кишечная непроходимость
Кишка, как уже говорилось выше, представляет собой полую трубку. Если в каком-либо отделе появляется препятствие (как внутри просвета, так и сдавливание извне), прохождение каловых масс по кишке прекращается и развивается картина непроходимости кишечника. Проявлением этого состояния будут схваткообразные боли в животе, вздутие живота, отсутствие стула и газов, сухость во рту, тошнота, повышение температуры тела. Одной из причин кишечной непроходимости может быть опухоль толстой кишки. Это состояние является поводом для экстренной госпитализации в хирургическое отделение.
Перфорация толстой кишки
Симптомы, позволяющие заподозрить рак ободочной кишки, весьма разнообразны. Они отличаются для рака правых и левых отделов ободочной кишки, порой не оказывают на жизнь человека особого влияния и могут быть проигнорированы или вовсе незамечены. Если говорить не только о раке ободочной кишки, но об онкологических заболеваниях в целом, можно разделить все симптомы на «общие» и «частные». Частные являются проявлением роста опухоли и отражают нарушение функции вовлеченного в опухолевый процесс органа или структуры. Общие симптомы неспецифичны, характерны для множества заболеваний, но как сами по себе, так и в сочетании с другими симптомами должны насторожить и заставить провести обследование.
Общие симптомы рака ободочной кишки
Самым частым общим симптомом является слабость и утомляемость. Если вы заметили у себя непривычную усталость при обычной нагрузке, это уже является поводом задуматься о своем здоровье и обратиться к специалистам. Головокружение, бледность кожных покровов обычно свидетельствуют об анемии, которая является вечной спутницей онкологических заболеваний. Насторожить должна и потеря веса, которая тоже часто сопровождает злокачественный процесс в организме.
Частные симптомы рака ободочной кишки
Опухоль ободочной кишки может проявлять себя нарушениями пищеварения, ощущением дискомфорта в животе, вздутием живота, изменением характера стула, появлением примесей крови и слизи к стулу, небольшим повышением температуры тела. Вопреки распространенному среди пациентов мнению, боли являются не самым частым и не самым характерным признаком рака и могут появляться только на поздних стадиях заболевания. Любые из перечисленных симптомов являются поводом для обращения к врачу-колопроктологу и проведения обследования для выявления заболевания, вызвавшего эти симптомы.
Диагностика рака ободочной кишки
Биопсия
Основным методом, позволяющим со стопроцентной уверенностью сказать, что у пациента рак ободочной кишки, является гистологическое исследование фрагмента опухоли. Чтобы подтвердить злокачественный характер опухолевого роста, необходимо исследовать опухолевую ткань под микроскопом. Это исследование проводится после получения материала во время колоноскопии с биопсией.
Колоноскопия
Ректороманоскопия
Ирригоскопия
Ирригоскопия – рентгенологическое исследование, в ходе которого выполняют несколько снимков ободочной кишки. Для того, чтобы кишку было видно на рентгеновском снимке, ее заполняют рентгенконтрастным веществом (вводят при помощи клизмы). Первый снимок делается при наполненной кишке. После опорожнения кишки ее раздувают воздухом и повторяют снимки. Это исследование позволяет выявить и достоверно определить локализацию опухоли.
Компьютерная томография (КТ)
КТ – рентгеновское сканирование какой–либо анатомической области, в результате которого делается множество снимков с небольшим интервалом. Пациентам с опухолью ободочной кишки показано выполнение компьютерной томографии двух областей – брюшной полости и грудной клетки, причем исследование брюшной полости обязательно должно быть выполнено с внутривенным контрастированием. Это исследование является золотым стандартом диагностики рака ободочной кишки, позволяет определить распространение опухоли, заподозрить наличие пораженных опухолевыми клетками лимфатических узлов, выявить отдаленные метастазы. Кроме того, выполненная на основе КТ 3D-реконструкция строения сосудов позволяет запланировать ход операции с учетом индивидуальных особенностей пациента. Компьютерная томография проводится в отделении лучевой диагностики, во время проведения исследования пациенту предложат лечь на специальную каталку, проезжающую через большую круглую катушку. Перед исследованием устанавливают венозный катетер, через который будет вводиться контрастный препарат. Очень важно получить от специалистов лучевой диагностики не только письменное заключение, но и диск с записанным исследованием. Компьютерная томография позволяет ответить на многие вопросы, определяющие тактику лечения. После исследования Вы должны предоставить заключение лучевого диагноста и диск с файлами врачу-колопроктологу для ознакомления с заключением и изучением диска. В Клинике колопроктологиии и малоинвазивной хирургии все специалисты владеют знаниями и умениями по изучению КТ-исследования.
ПЭТ-КТ
В некоторых случаях для уточнения распространенности опухолевого процесса может понадобиться выполнение позитронно-эмиссионной томографии (ПЭТ-КТ). Это исследование похоже на обычную томографию, но проводится с использованием особого контрастного вещества, которое будет видно на снимках в тех тканях, в которых происходит усиленный обмен веществ. Некоторые органы в норме накапливают контраст, например, мочевой пузырь, почки и головной мозг, но для опухолевых клеток особенно характерен ускоренный обмен веществ, поэтому данное исследование позволяет увидеть даже самые маленькие опухолевые отсевы – как в лимфатические узлы, так и в другие органы.
УЗИ и рентгенография брюшной полости
Ультразвуковое исследование и рентгенография не являются золотым стандартом для диагностики опухолей ободочной кишки и определения стадии опухолевого процесса, но применяется для диагностики острых осложнений рака ободочной кишки.
МРТ органов брюшной полости
Магнитно-резонансная томография брюшной полости не является стандартным исследованием для опухолей ободочной кишки, но в случае метастатического поражения печени (или на его подозрения) необходима для определения характеристик очаговых образований в печени и решения вопроса о дальнейшей тактике лечения.
Лабораторные исследования
Общий и биохимический анализы крови, коагулограмма (исследование свертываемости крови) и общий анализ мочи являются обязательными при обследовании пациентов с онкологическими заболеваниями и позволяют оценить общее состояние организма.
Онкомаркеры
Исследования крови на онкомаркеры (особые вещества, вырабатываемые опухолью) выполняются всем пациентам с колоректальным раком. Положительные результаты не являются основанием для постановки диагноза, но указывают на необходимость дообследования. При установленном диагнозе «колоректальный рак» значения этих анализов позволяют косвенно оценить прогноз. Наиболее информативными для колоректального рака являются онкомаркеры: CA19-9 и РЭА.
Дополнительные исследования
Исследование кала на скрытую кровь является простым и быстрым методом скрининга колоректального рака, но, к сожалению, не самым достоверным. Вероятность ложноположительного результата высока, может быть связана с особенностями питания, любыми другими причинами скрытых кровотечений в ЖКТ, даже с травмой десны при чистке зубов в день исследования. Для того, чтобы выяснить причину положительного результата теста на скрытую кровь, необходимо более полное обследование.
Виртуальная колоноскопия – это метод, объединяющий компьютерную томографию и ирригоскопию, но не обладающий преимуществами обычной колоноскопии. После подготовки кишки проводится компьютерная томография, при этом толстую кишку раздувают воздухом. После исследования специалисты по лучевой диагностике выполняют 3Д-реконструкцию просвета кишечника, что позволяет осмотреть всю толстую кишку «изнутри», однако при подозрении на какие-либо изменения необходимо проведение колоноскопии и биопсии.
Гастроскопия должна выполняться всем пациентам с колоректальным раком не только для исключения синхронного поражения желудка, но и для выявления (и при необходимости последующего лечения) гастрита и язвенной болезни пациентам в рамках предоперационной подготовки и лечения.
Что делать, если установлен диагноз рак ободочной кишки?
С точки зрения психологов, человек, столкнувшийся со сложной ситуацией в жизни, в том числе с выявлением тяжелого заболевания, проходит через 5 стадий:
Стадии рака ободочной кишки и способы лечения
Единственным радикальным методом лечения рака ободочной кишки является хирургический метод. Только выполнение операции по удалению опухоли и лимфатических узлов позволяет полностью удалить все проявления злокачественного процесса (при резектабельном раке). Дополнением к операции является химиотерапия, которая может проводиться как до операции, так и после при наличии определенных показаний. Прежде чем подробно говорить о лечении, следует разобраться в стадиях колоректального рака. Выше были описаны особенности роста первичной опухоли и пути метастазирования колоректального рака, и именно они определяют стадию заболевания.
Существует классификация TNM, обозначающая распространение первичной опухоли (Т), наличие пораженных лимфатических узлов (N) и отдаленных метастазов (М). Кроме этих существуют дополнительные индексы, которые могут использоваться при формулировке диагноза, однако именно значения названных выше трех индексов обозначают клиническую стадию. Всего выделяют четыре стадии колоректального рака, чем выше порядковый номер стадии, тем выраженнее распространение опухоли.
Стадия может быть установлена клинически (то есть только при использовании инструментальных методов обследования) и морфологически (после исследования удаленной кишки и лимфатических узлов под микроскопом), это обозначается индексами «с» и «р» соответственно. Морфологическое исследование обладает наибольшей достоверностью, чем все инструментальные методы диагностики вместе взятые, и поэтому стадия может измениться после операции как в меньшую, так и в большую сторону, и это не является ошибкой диагностики.
При лечении опухолей 0 и I стадии возможно местное иссечение опухоли – малоинвазиваная эндоскопическая операция. Она выполняется при колоноскопии под наркозом, разрезы на передней брюшной стенке не выполняются. После операции необходимо наблюдаться несколько дней в стационаре и соблюдать щадящую диету. После получения результатов морфологического (иными словами – гистологического) исследования возможны два варианта дальнейшей тактики. На основании заключения морфолога определяются факторы прогноза. При отсутствии неблагоприятных факторов возможно ограничиться только наблюдением по программе послеоперационного мониторинга, однако при наличии неблагоприятных факторов пациенту будет предложена операция по удалению участка кишки и лимфатических узлов. Окончательное решение принимается на онкологическом консилиуме, где также учитывается мнение пациента.
Лечение опухолей II-III стадии заключается в удалении участка кишки с опухолью и всех регионарных лимфатических узлов, такая операция может быть выполнена любым способом – роботическим, лапароскопическим или открытым. Иногда до операции назначается проведение нескольких курсов химиотерапии для улучшения результатов оперативного лечения. Количество удаленных лимфатических узлов – важнейший фактор прогноза, даже при отсутствии их поражения, это еще одно из преимуществ выполнения расширенной лимфодиссекции. Удаление и обнаружение в препарате менее 12 лимфатических узлов по современным стандартам является неприемлемым в лечении колоректального рака.
После операции препарат (кишка и лимфоузлы) направляются в морфологическую лабораторию, исследуются под микроскопом. После получения результата возможны следующие варианты лечения:
В некоторых случаях необходимо дообследование – проведение иммуногистохимического и/или генетического исследования (определение микросателлитной нестабильности), позволяющего предсказать прогноз и ответ на химиотерапию.
Лечение колоректального рака IV стадии – наиболее неблагоприятной по отдаленным результатам, является спорным и дискутабельным вопросом. Пациенты с IV стадией составляют разнородную группу, отличающуюся по многим факторам, которые могут определять прогноз – количество и размеры метастазов, их локализация, размеры и локализация первичной опухоли, степень проявления симптомов опухоли и метастазов, наличие пораженных лимфатических узлов, наличие генетических мутаций в опухоли. В данной группе возможно химиотерапевтическое, хирургическое (в том числе эндоскопическое) лечение, воздействие на метастазы высокотехнологическими способами и, конечно, комбинации этих методов лечения. В современных рекомендациях для данной стадии прописано следующее: показано проведение химиотерапии, но возможно и хирургическое лечение. Учитывая разнообразные проявления заболевания и разные факторы прогноза, при лечении рака ободочной кишки IV стадии необходим индивидуальный подход, а решение о лечении должно приниматься коллегиально, на онкологическом консилиуме.
В первую очередь пациентов с раком ободочной кишки IV стадии следует разделить на следующие группы: пациенты с резектабельными, условно-резектабельными и нерезектабельными метастазами. Первая из этих групп имеет наиболее благоприятный прогноз, в данном случае возможно как удаление опухоли ободочной кишки с лимфатическими узлами и метастазов во время одной операции, так и разделение этих этапов на две операции.
Пациентам с условно-резектабельными метастазами показано проведение химиотерапевтического лечения с последующей оценкой динамики изменения метастазов, и при достижении резектабельного состояния метастазов – операция по удалению всех проявлений опухолевого процесса. После операции всем пациентам с IV стадией показано проведение химиотерапии при отсутствии противопоказаний. Схематично можно разбить все лечение пациентов с условно-резектабельными и резектабельными метастазами на блоки: «химиотерапии до операции», «операция по поводу опухоли толстой кишки», «операция по поводу отдаленных метастазов», «химиотерапия после операции», и, комбинируя эти блоки, можно представить, сколько последовательностей этапов лечения возможно в этой группе пациентов. Только командный подход, оценка всех факторов рисков, привлечение врачей разных специальностей к обсуждению каждой клинической ситуации позволяет выбрать правильную стратегию лечения.
Для пациентов с нерезектабельными метастазами возможны две опции лечения – комбинация хирургической операции по поводу опухоли кишки с химиотерапией или только химиотерапевтическое лечение. Согласно данным исследований многих зарубежных авторов, при IV стадии колоректального рака с нерезектабельными метастазами операция по удалению первичной опухоли в комбинации с химиотерапевтическим лечением улучшает результаты по сравнению с проведением только химиотерапии.
К сожалению, бывают такие ситуации, когда и метастазы, и первичная опухоль являются неудаляемыми хирургически. В таком случае возможно проведение химиотерапии с последующей оценкой возможности выполнения хирургического лечения, а так же выполнение операций, облегчающих состояние пациента и улучшающих качество жизни.
Операции, выполняемые при раке ободочной кишки
Все радикальные и условно-радикальные операции при раке ободочной кишки можно схематично представить следующим образом:
Прочитать подробно про роботические, лапароскопические и открытые операции возможно в соответствующих разделах нашего сайта.
При колоректальном раке выполняются следующие операции:
Правосторонняя гемиколэктомия – удаление правой половины ободочной кишки с конечным участком тонкой кишки. Выполняется при раке восходящей ободочной кишки, локализации опухоли в слепой кишке, печеночном изгибе ободочной кишки, раке изгиба ободочной кишки.
Резекция поперечно-ободочной кишки выполняется при раке поперечной ободочной кишки, может сопровождаться лимфодиссекцией вдоль двух систем сосудов, поскольку кровоснабжается поперечно-ободочная кишка за счет ветвей и верхней, и нижней брыжеечной артерии.
Левосторонняя гемиколэктомия – удаление левой половины ободочной кишки, в настоящее время выполняется редко, преимущество отдается резекции левых отделов, причем длина удаленного участка кишки определяется локализацией опухоли и строением сосудов. Левосторонняя гемиколэктомия в современном мире используется при синхронном поражении левых отделов ободочной кишки несколькими опухолями.
Резекция левых отделов ободочной кишки выполняется при локализации опухоли в селезеночном изгибе, нисходящей ободочной кишке и проксимальной трети сигмовидной кишки.
Резекция сигмовидной кишки выполняется при опухолевом поражении средней трети сигмовидной кишки.
Все операции по поводу колоректального рака в нашей клинике выполняются с расширенной лимфодиссекцией, то есть с удалением лимфатических узлов всех трех порядков. Такой подход заимствован нами из Японской онкологии, страны, являющейся лидером по лечению онкологических заболеваний. Расширенная лимфодиссекция позволяет улучшить результаты лечения по сравнению с обычной и тем более неопределенной лимфодиссекцией, к сожалению, до сих пор выполняемой в отечественных учреждениях. Удаление большего количества лимфатических узлов позволяет достоверно определить стадию и улучшить прогноз лечения колоректального рака.
Реконструктивный этап – формирование анастомоза – может выполняться как вручную (участки кишки сшиваются нитками), так и механически – с использованием специальных сшивающих аппаратов (участки кишки скрепляются скобками). В тех случаях, когда существуют риски несостоятельности анастомоза (системные заболевания, связанные с нарушением микроциркуляции, плохая подготовка толстой кишки при частичном нарушении кишечной проходимости) формируется превентивная стома – на переднюю брюшную стенку выводится петля кишки. Это позволяет отключить пассаж по кишке и дать анастомозу время зажить, а после – выполнить реконструктивную операцию и вернуть естественный ход кишечному содержимому. Надо отметить, что при раке ободочной кишки превентивная стома формируется значительно реже, чем при раке прямой кишки, когда ее формирование при определенных локализациях опухоли запланировано заранее.
Что делать если опухоль удалить невозможно?
При невозможности выполнения операций вышеуказанного объема (например, в экстренной ситуации при осложненном течении заболевания или при нерезектабельной первичной опухоли) выполняются симптоматические операции, которые могут стать «мостом» к проведению более радикального лечения. К таким операциям относится:
Если одна из таких операций была выполнена, не стоит считать, что на этом лечение окончено. Возможности хирургического лечения зависят не только от распространенности опухолевого процесса и наличия осложнений, но и от оснащения операционной и уровня подготовки хирургов, причем последние два аспекта в хирургическом отделении городской больницы, к сожалению, могут отличаться от оснащенной по последнему слову техники клиники, сотрудники которого ежедневно сталкиваются с онкологическим заболеванием. После восстановительного периода следует обратиться к онкологу или колопроктологу для дообследования, решения вопроса о дальнейшем лечении и никогда не стоит пренебрегать возможностью обратиться за еще одним мнением специалистов.
Подготовка к операции
После того, как завершено обследование, установлена стадия, принято решение о хирургическом вмешательстве, наступает основной этап лечения – операция. Это волнительное и даже пугающее событие, и каждый человек переживает перед операцией, но понимание самого процесса лечения и, главное, его необходимости обычно способствует улучшению эмоционального фона. Подготовка к операции может начинаться задолго до госпитализации, если необходима компенсация проявлений сопутствующих заболеваний. На данном этапе подготовку контролируют анестезиологи и терапевты. Не стоит скрывать наличие хронических заболеваний и бояться, что это может стать причиной отказа в операции. Плановые операции, даже по поводу онкологических заболеваний, в большинстве случаев можно перенести на некоторое время, необходимое для лечения сопутствующих заболеваний, обострение которых может привести к осложнениям во время или после операции. После операции по поводу рака ободочной кишки требуется ношение компрессионных чулок и бандажа на переднюю брюшную стенку, об их наличии лучше позаботиться до операции. После госпитализации, уже в стационаре, осуществляются последние этапы подготовки – очистка кишки и бритье области операции.
Операция
Послеоперационный период
Самое главное правило послеоперационного периода – ранняя активизация. После перевода в палату нужно обязательно садиться в постели, делать дыхательную гимнастику, вставать, ходить по палате и по отделению – как можно больше двигаться. Это способствует восстановлению перистальтики кишечника, а также является профилактикой осложнений со стороны дыхательной системы и тромбоэмболических осложнений. Особенности питания после операции достаточно индивидуальны, диету в послеоперационном периоде назначает и контролирует лечащий врач. Обычно первое время следует употреблять в пищу все жидкое и перетертое, затем можно расширять рацион. В послеоперационном периоде остается подключичный и эпидуральный катетер, установленный до операции, через него будут вводиться лекарственные вещества. Мочевой катетер убирается при переводе в отделение, если нет показаний для его более длительного применения. Обычно после операции устанавливается дренаж – полая трубка – через отверстие в правом или левом боку, который убирается через несколько дней после операции при отсутствии показаний к его более длительному стоянию. В отделении выполняются перевязки, проводится лекарственная терапия. Постепенно все катетеры и дренажи убираются и пациент готовится к выписке. Сроки госпитализации индивидуальны, определяются особенностями операции и течением послеоперационного периода.
Жизнь после операции
После выписки из стационара и получения результатов гистологического исследования определяется дальнейшая тактика лечения. Несмотря на то, что пациенты возвращаются к привычному ритму жизни или сразу после операции, или после проведения послеоперационной химиотерапии, забывать об этом заболевании не следует. Всем пациентам, оперированным по поводу рака ободочной кишки, необходимо проходить контрольные обследования по программе мониторинга, которые необходимо учитывать при планировании своего расписания и проходить регулярно.
Разработанная в нашей клинике программа предусматривает прохождение обследований каждые три месяца и направлена на раннее выявление возможной прогрессии или рецидива рака ободочной кишки. Мы стремимся поддерживать контакт со всеми нашими пациентами после операции, поэтому не стоит удивляться, если ваш лечащий врач или сотрудник отдела послеоперационного мониторинга будет звонить или писать вам письма на электронную почту и интересоваться результатами обследований после операции. Своевременное прохождение послеоперационного мониторинга под контролем вашего лечащего врача – залог успешного лечения.
Часто задаваемые вопросы
Какова продолжительность жизни при раке ободочной кишки?
Предсказать, сколько составит продолжительность жизни, достоверно нельзя. Существуют показатели 5-летней выживаемости (вероятность прожить 5 лет), которые напрямую зависят от стадии заболевания и проведенного лечения. Кроме того, существуют факторы благоприятного и неблагоприятного прогноза течения заболевания. Узнать о прогнозе заболевания можно у вашего лечащего врача, который знаком со всеми данными вашей клинической ситуации.
Смогу ли я вернуться к обычной жизни после лечения?
Все пациенты возвращаются к привычному ритму жизни. Первое время после операции будут ограничения по физической активности и диете, однако постепенно эти ограничения будут сняты. Проведение химиотерапии, если оно показано, означает двухдневную госпитализацию каждые две недели в течение полугода (или реже и короче при других схемах химиотерапии). Проведение обследований по программе мониторинга с последующей консультацией возможно за один день амбулаторно, то есть без госпитализации в стационар.
Следует ли говорить родственникам о заболевании?
Этот вопрос каждый пациент решает для себя сам. При госпитализации пациент подписывает согласие о сообщении сведений о своем здоровье, где может указать, кто из родственников может общаться с лечащим врачом и получать информацию. Прежде чем принять это решение, следует учесть, что после операции вам может потребоваться помощь и поддержка близких людей.
Следует ли говорить родственнику, что он болен?
Этот этический вопрос регулируется федеральным законом.
Каждый имеет право получить в доступной для него форме имеющуюся в медицинской организации информацию о состоянии своего здоровья, в том числе сведения о результатах медицинского обследования, наличии заболевания, об установленном диагнозе и о прогнозе развития заболевания, методах оказания медицинской помощи, связанных с ними рисках, возможных видах медицинского вмешательства, его последствиях и результатах оказания медицинской помощи.
Информация о состоянии здоровья не может быть предоставлена пациенту против его воли. В случае неблагоприятного прогноза развития заболевания информация должна сообщаться в деликатной форме пациенту или его супругу (супруге), одному из близких родственников (детям, родителям, усыновленным, усыновителям, родным братьям и родным сестрам, внукам, дедушкам, бабушкам), если пациент не запретил сообщать им об этом и (или) не определил иное лицо, которому должна быть передана такая информация.
Что делать, если отказали в операции?
Не бойтесь обратиться в другое учреждение. Каждая клиническая ситуация должна рассматриваться индивидуально, а тактика лечения должна быть выбрана на онкологическом консилиуме
Что такое онкологический консилиум?
Это совещание врачей нескольких специальностей, принимающих участие в обследовании и лечении пациента с онкологическим заболеванием. В нашей клинике для определения стратегии лечения больных колоректальным раком регулярно встречаются специалисты лучевой диагностики, эндоскописты, химиотерапевты, хирурги, лучевые терапевты, анестезиологи и морфологи. При необходимости приглашаются специалисты узкого профиля (гинекологи, урологи, кардиохирурги). Любой пациент с колоректальным раком может обратиться в нашу клинику, даже если проходит лечение в другом учреждении, и тактика лечения будет определена коллегиально. Подробнее об онкологическом консилиуме можно узнать здесь.
Что делать, если прооперировали в экстренном порядке в хирургическом отделении?
Необходимо обратиться в онкологический диспансер или профильное для данного заболевания учреждение. Операция, выполненная по экстренным показаниям, может быть не радикальной, соответственно, может потребоваться выполнение второй операции или другое дополнительное лечение.
Что делать, если вывели стому?
При раке ободочной кишки редко формируют постоянную стому. Возможно выполнение реконструктивно-восстановительной операции, подробнее можно узнать в соответствующем разделе сайта и на консультации у наших врачей
Есть ли альтернатива хирургическому и химиотерапевтическому лечению?
Нет. Опасайтесь мошенников, которые предлагают методы «народной медицины». К сожалению, эти нечестные люди обладают хорошим даром убеждения и могут привлечь пациентов к «лечению» абсолютно неэффективными и вредными методами. Даже если употребление трав, молитв, мочи или других методов «лечения» не принесет особого вреда вашему организму, будет упущено время и заболевание может распространиться настолько, что радикальное лечение будет невозможно. Игнорируйте такие предложения, не доверяйте информации из непроверенных источников и в первую очередь задайте все интересующие вас вопросы о вашем заболевании и его лечении специалисту.
Как проходит химиотерапия?
Введение химиопрепаратов происходит внутривенно, возможна комбинация таблетированных и инъекционных форм. Для проведения химиотерапии возможна установка специальной внутривенной порт-системы.
Какие осложнения химиотерапии возможны? Выпадут ли волосы?
При применении схем химиотерапии для колоректального рака такого побочного эффекта, как облысение, нет. Возможны побочные реакции: тошнота, рвота, диарея, сыпь на кожных покровах, нарушение чувствительности дистальных отделов конечностей, анемия и лейкопения. При появлении выраженных побочных реакций проводят снижение дозы или смену схемы химиотерапии.
Что делать, если во время операции не были удалены лимфатические узлы?
Во-первых, возможно рассмотрение выполнения повторной операции. Во-вторых, это является показанием для химиотерапии, если после первой операции не прошло более двух месяцев и нет противопоказаний к химиотерапии. В такой ситуации следует обратиться в специализированное учреждение на консультацию для определения тактики лечения или участия в онкоконсилиуме.
Часто ли бывают рецидивы?
При проведении радикального лечения по современным стандартам их частота сводится к минимальной. Для того, чтобы вовремя распознать и вылечить рецидив, необходимо наблюдение по программе мониторинга.
Какие бывают осложнения после операции?
К сожалению, после операции иногда бывают осложнения. Некоторые из них даже могут потребовать повторной операции. Возможны осложнения со стороны послеоперационной раны, деокмпенсация сопутствующих заболеваний, кровотечение, несостоятельность анастомоза. Команда нашей клиники делает все возможное, чтобы избежать осложнений в послеоперационном периоде.
Кто будет ухаживать после операции?
За пациентами после операций ухаживает младший и средний медицинский персонал, а также родственники пациента. При необходимости возможен индивидуальный пост – медицинская сестра, которая в течение суток уделяет время одному пациенту.
Какие условия в палате?
Все палаты нашей клиники комфортны и полностью оснащены для послеоперационных пациентов.
Как попасть на прием в нашу клинику?
В Клинику колопроктологии и малоинвазивной хирургии может обратиться любой человек, которому требуется лечение органов толстой кишки, анального канала и промежностей. Для первичной консультации необходимо записаться на прием у администраторов Клиники.






